题目内容
17.下列实验方案中,不能达到实验目的是( )| A. | 鉴别硬水和软水----加肥皂水搅拌 | |
| B. | 除去氯化钠固体中的少量碳酸钠----加入适量稀盐酸,充分反应后,蒸发 | |
| C. | 分离碳酸钠和氢氧化钠的混合物----加入过量氯化钙溶液,过滤 | |
| D. | 区分羊毛与合成纤维----点燃,闻气味 |
分析 A、根据硬水和软水的区别进行分析判断;
B、根据碳酸钠和稀盐酸反应产生氯化钠、水和二氧化碳进行分析;
C、根据碳酸钠能够和氯化钙反应产生碳酸钙沉淀结合分离的原理进行分析;
D、根据羊毛灼烧会产生烧焦羽毛气味的气体进行分析.
解答 解:A、硬水是含有较多钙、镁离子的水,加肥皂水产生的泡沫较少,而软水加肥皂水产生的泡沫较多,可以鉴别,故选项实验方案能达到实验目的;
B、碳酸钠和稀盐酸反应产生氯化钠、水和二氧化碳,然后通过蒸发可以得到氯化钠,故选项实验方案能达到实验目的;
C、碳酸钠能够和氯化钙反应产生碳酸钙沉淀,过量的氯化钙会增加新的杂质,不能将二者分离,故选项实验方案不能达到实验目的;
D、取样品,分别灼烧,有烧焦羽毛气味的气体产生的是羊毛,没有此气味产生的是棉线,现象不同,可以鉴别,故选项实验方案能达到实验目的;
故选项为:C.
点评 本题难度不大,化学实验方案的设计是考查学生能力的主要类型,同时也是实验教与学难点,在具体设计时要对其原理透彻理解,可根据物质的物理性质和化学性质结合实验目的进行分析判断.

练习册系列答案
相关题目
8.下列相同质量的金属,原子数目最少的是( )
| A. | Mg | B. | Al | C. | Na | D. | Ca |
2.学习了二氧化锰对过氧化氢分解有催化作用的知识后,某同学想:氧化铜能否起到类似二氧化锰的催化剂作用呢?于是进行以下探究.
【猜想】Ⅰ、氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2g氧化铜(CuO),取5mL5%的过氧化氢溶液于试管中,
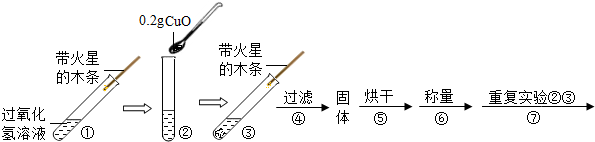
进行实验:
(1)填写下表:
(2)步骤①的目的是与步骤③对照.
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.所缺仪器在此步骤中的作用是引流.
(4)过氧化氢能被氧化铜催化分解放出氧气的化学方程为2H2O2$\frac{\underline{\;氧化铜\;}}{\;}$2H2O+O2↑.
【猜想】Ⅰ、氧化铜不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、氧化铜参与反应产生氧气,反应前后质量和化学性质发生了改变;
Ⅲ、氧化铜是反应的催化剂,反应前后质量和化学性质不变.
【实验】用天平称量0.2g氧化铜(CuO),取5mL5%的过氧化氢溶液于试管中,

进行实验:
(1)填写下表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 有气泡产生, 带火星的木条复燃 | 称量的氧化铜的质量仍为0.2g | 溶液中有气泡, 带火星的木条复燃. | 猜想Ⅰ、Ⅱ不成立;猜想Ⅲ成立. |
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.所缺仪器在此步骤中的作用是引流.
(4)过氧化氢能被氧化铜催化分解放出氧气的化学方程为2H2O2$\frac{\underline{\;氧化铜\;}}{\;}$2H2O+O2↑.
6.下列各物质的变化中,属于分解反应的是( )
| A. | 水$\stackrel{通电}{→}$氢气+氧气 | B. | 碳+氧气$\stackrel{点燃}{→}$二氧化碳 | ||
| C. | 铝+氧气$\stackrel{点燃}{→}$氧化铝 | D. | 乙炔+氧气$\stackrel{点燃}{→}$二氧化碳+水 |
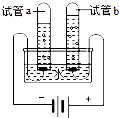 (1)水是人类最宝贵的自然资源,多一滴水,就可能多一条生命.小明利用右图所示的装置探究水的组成.通电一段时间后,试管a收集到的气体是氢气,试管b收集到的气体是氧气,其体积之比约为2:1,该实验中发生反应的符号表达式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,其反应类型是分解反应.
(1)水是人类最宝贵的自然资源,多一滴水,就可能多一条生命.小明利用右图所示的装置探究水的组成.通电一段时间后,试管a收集到的气体是氢气,试管b收集到的气体是氧气,其体积之比约为2:1,该实验中发生反应的符号表达式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,其反应类型是分解反应. 2013年12月15日,嫦娥三号成功与玉兔号月球车互拍,五星红旗亮相月面.嫦娥三号任务成功实施,使中国成为世界上第三个掌握月球软着陆和月面巡视探测技术的国家.
2013年12月15日,嫦娥三号成功与玉兔号月球车互拍,五星红旗亮相月面.嫦娥三号任务成功实施,使中国成为世界上第三个掌握月球软着陆和月面巡视探测技术的国家. 为测定空气的成分按如图所示进行实验:
为测定空气的成分按如图所示进行实验: