题目内容
17.“84消毒液”广泛应用于物体表面的消毒,其有效成分是次氯酸钠,现有50g质量分数10%的次氯酸钠溶液,欲将其质量分数提高一倍,需要加入多少克次氯酸钠?分析 现有50g质量分数10%的次氯酸钠溶液,欲将其质量分数提高一倍,即变为20%,据此结合溶质质量=溶液质量×溶质的质量分数,进行分析解答.
解答 解:现有50g质量分数10%的次氯酸钠溶液,欲将其质量分数提高一倍,设需要加入次氯酸钠的质量为x,
(50g+x)×20%=50g×10%+x,x=6.25g.
答:需要加入6.25g次氯酸钠.
点评 本题难度不是很大,考查溶液的浓缩问题,掌握溶液浓缩的方法、原理是正确解答此类题的关键所在.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
7.对于下列几种化学符号,有关说法正确的是( )
①H ②Fe2+ ③Cu ④N2O5 ⑤Fe3+ ⑥NaCl.
①H ②Fe2+ ③Cu ④N2O5 ⑤Fe3+ ⑥NaCl.
| A. | 能表示一个分子的是①④⑥ | |
| B. | 表示物质组成的化学式是③④⑥ | |
| C. | ②⑤的质子数相同,化学性质也相同 | |
| D. | ④中的数字“5”表示五氧化二氮中有5个氧原子 |
8.下列变化中,属于化学变化的是( )
| A. | 石蜡融化 | B. | 酒精燃烧 | C. | 铁丝弯曲 | D. | 西瓜榨汁 |
5.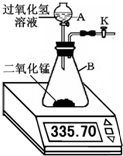 现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):
现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):
请根据要求回答下列问题:
①生成氧气的物质的量为0.05mol;
②根据上述氧气的量计算参加反应的过氧化氢的质量(根据化学方程式列式计算)
3.4g.
 现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):
现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 装置+过氧化氢溶液 +二氧化锰/g | 335.70 | 335.68 | 335.54 | 335.18 | 334.46 | 334.10 | 334.10 |
①生成氧气的物质的量为0.05mol;
②根据上述氧气的量计算参加反应的过氧化氢的质量(根据化学方程式列式计算)
3.4g.
6.海洋是人类巨大的资源宝库,海洋资源的开发前景十分广阔.下列有关海洋的叙述错误的是( )
| A. | 海底蕴藏着大量的煤、石油和天然气等矿产资源 | |
| B. | 常用于淡化海水的方法有蒸馏法、过滤法等 | |
| C. | 海水中盐的质量分数约为3.5% | |
| D. | 海水中含量最多的元素是氧元素 |