题目内容
10.豆浆被称为“植物奶”,其中含有的异黄酮“C15H10O2)具有防癌功能,下列说法正确的是( )| A. | 异黄酮中共含有27个原子 | |
| B. | 异黄酮中碳元素质量分数最大 | |
| C. | 异黄酮中C、H、O三种元素的质量比为15:10:2 | |
| D. | 异黄酮的化学式量为222g |
分析 A.根据异黄酮(C15H10O2)化学式的含义进行分析判断.
B.根据化合物中元素的质量分数的比较方法来分析;
C.根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析;
D.根据相对分子质量的单位来分析.
解答 解:A.根据异黄酮(C15H10O2)化学式可知,一个异黄酮分子中含有27个原子,故错误;
B.异黄酮中C、H、O三种元素的质量比为(12×15):(1×10):(16×2)=90:5:16,由此可见其中碳元素的质量分数最大,故正确;
C.异黄酮中碳、氢、氧元素的质量比为(12×15):(1×10):(16×2)≠15:10:2,故错误;
D.相对分子质量单位是“1”,不是“克”,常常省略不写,故错误.
故选B.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义、有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
20.甲同学误把H2O2溶液当作酸与Fe2O3粉末混合,发现有大量气泡产生,他联想到MnO2可作为H2O2分解的催化剂,那么Fe2O3能否作为H2O2分解的催化剂呢?请你一起参探究,并填写下列空白:
[猜想]Fe2O3能作为H2O2分解的催化剂
[实验验证]甲同学依次设计了三个实验:
实验一 取一定量的H2O2溶液于试管中,观察到有及少量气泡产生,伸入带火星的木条,木条复燃,说明H2O2溶液常温下缓慢分解.
实验二 在实验一的试管中加入Wg Fe2O3粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃,说明Fe2O3能加快H2O2的分解速率.
实验三 待反应结束后,将试管离得不溶物滤出,并洗涤、干燥、称量,固体质量仍为Wg,说明反应前后Fe2O3的质量保持不变.
[实验结论]甲同学认为,Fe2O3粉末可以作为H2O2分解的催化剂
[反思评价]乙同学认为要证明甲同学的结论正确,仅做这三个实验还不充分,需要再补充一个探究实验,探究反应前后Fe2O3的化学性质是否改变.
[拓展]下表是丙同学探究影响H2O2分解因素时所记录的部分数据,通过对数据分析,你能得出什么结论?相同条件下,MnO2的催化效果比Fe2O3好.
用足量等体积H2O2溶液制取相同体积O2所需的时间(分钟):
[猜想]Fe2O3能作为H2O2分解的催化剂
[实验验证]甲同学依次设计了三个实验:
实验一 取一定量的H2O2溶液于试管中,观察到有及少量气泡产生,伸入带火星的木条,木条复燃,说明H2O2溶液常温下缓慢分解.
实验二 在实验一的试管中加入Wg Fe2O3粉末,有大量气泡产生,然后伸入带火星的木条,木条复燃,说明Fe2O3能加快H2O2的分解速率.
实验三 待反应结束后,将试管离得不溶物滤出,并洗涤、干燥、称量,固体质量仍为Wg,说明反应前后Fe2O3的质量保持不变.
[实验结论]甲同学认为,Fe2O3粉末可以作为H2O2分解的催化剂
[反思评价]乙同学认为要证明甲同学的结论正确,仅做这三个实验还不充分,需要再补充一个探究实验,探究反应前后Fe2O3的化学性质是否改变.
[拓展]下表是丙同学探究影响H2O2分解因素时所记录的部分数据,通过对数据分析,你能得出什么结论?相同条件下,MnO2的催化效果比Fe2O3好.
用足量等体积H2O2溶液制取相同体积O2所需的时间(分钟):
| 浓度 时间 催化剂 | 30% H2O2溶液 | 15% H2O2溶液 | 5% H2O2溶液 |
| 加入WgMnO2 | 0.2 | 0.8 | 2.0 |
| Wg Fe2O3 | 7.0 | 9.0 | 16.0 |
18.下列物质的用途只是由其化学性质决定的是( )
| A. | 石墨作电池的电极 | B. | 用氢气做燃料 | ||
| C. | 稀有气体充电发光 | D. | 用干冰做致冷剂 |
5.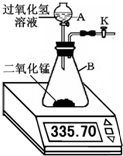 现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):
现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):
请根据要求回答下列问题:
①生成氧气的物质的量为0.05mol;
②根据上述氧气的量计算参加反应的过氧化氢的质量(根据化学方程式列式计算)
3.4g.
 现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):
现有如图的氧气发生装置,取34g过氧化氢溶液于分液漏斗A中,向B中加入一定量的二氧化锰,活塞K保持打开.不同时间电子天平的读数如下表所示(不考虑H2O逸出):| 反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 装置+过氧化氢溶液 +二氧化锰/g | 335.70 | 335.68 | 335.54 | 335.18 | 334.46 | 334.10 | 334.10 |
①生成氧气的物质的量为0.05mol;
②根据上述氧气的量计算参加反应的过氧化氢的质量(根据化学方程式列式计算)
3.4g.