题目内容
13.有一包固体样品可能含有氢氧化钠、碳酸钠、硫酸钠、硝酸钡、硫酸铜中的一种或几种.某化学兴趣小组为探究其成分做了以下实验:
Ⅰ.取少量固体于烧杯中,逐渐加水并不断搅拌至烧杯内固体不再溶解
Ⅱ.过滤,得到白色固体和无色清夜
Ⅲ.取少量清夜于试管中,滴加酚酞溶液,酚酞溶液不变色
请回答下列问题
(1)根据上述信息判断,该样品不可能含硫酸铜和氢氧化钠固体.
(2)提出合理假设,样品的成分有3种可能:
假设1:碳酸钠、硝酸钡 假设2:硫酸钠、硝酸钡 假设3:碳酸钠、硫酸钠、硝酸钡.
(3)为进一步探究固体样品的成分,该组同学取少量原固体于试管中.
限选试剂:稀盐酸、稀硫酸、稀硝酸、氯化钡溶液、蒸馏水
完成实验方案,请填写实验操作,与表中结论相符的预期现象.
| 实验操作 | 预期现象 | 结论 |
| 步骤1: 取少量原固体样品于试管中,逐渐加水并不断搅拌至烧杯内固体不再溶解 | 有白色固体 | 假设1成立 |
| 步骤2: 向步骤1反应后的白色固体中滴加足量稀稀HNO3溶液,并不断震荡 | 白色固体完全溶解,有气泡产生 |
分析 (1)由于白色粉末溶于水后能得到沉淀和溶液,溶液为无色,所以固体中一定不会含有硫酸铜,取少量清液于试管中,滴加酚酞溶液,酚酞溶液不变色,所以固体中一定不会含有氢氧化钠;
(2)由于固体中只可能含有碳酸钠、硫酸钠、硝酸钡三种物质,而碳酸钠、硫酸钠溶于水不能形成沉淀,所以样品的成分有3种可能,据此分析解答即可;
(3)由于取少量固体于烧杯中,逐渐加水并不断搅拌至烧杯内固体不再溶解,过滤,得到白色固体和无色清液,取少量清液于试管中,滴加酚酞溶液,酚酞溶液不变色;根据钡离子和碳酸根与硫酸根的反应验证分析.
解答 解:(1)由于白色粉末溶于水后能得到沉淀和溶液,溶液为无色,所以固体中一定不会含有硫酸铜,取少量清液于试管中,滴加酚酞溶液,酚酞溶液不变色,所以固体中一定不会含有氢氧化钠;由此知该样品不可能含硫酸铜和氢氧化钠固体;
(2)由于固体中只可能含有碳酸钠、硫酸钠、硝酸钡三种物质,而碳酸钠、硫酸钠溶于水不能形成沉淀,所以样品的成分有3种可能:除假设1、假设2以外,假设3应为:
碳酸钠、硫酸钠、硝酸钡;
(3)为进一步探究固体样品的成分,取少量原固体样品于试管中,逐渐加水并不断搅拌至烧杯内固体不再溶解,过滤,得到白色固体和无色清液,白色固体能够溶于稀HNO3溶液且生成气体,所以该沉淀不可能是硫酸钡,由此可判断假设1成立.
故答案为:
(1)硫酸铜;氢氧化钠;
(2)碳酸钠、硫酸钠、硝酸钡;
(3)
| 实验操作 | 预期现象 | 结论 |
| 取少量原固体样品于试管中,逐渐加水并不断搅拌至烧杯内固体不再溶解 | 有白色固体 | |
| 向步骤1反应后的白色固体中滴加足量稀稀HNO3溶液,并不断震荡 | 白色固体完全溶解,有气泡产生 |
点评 解答本题要掌握各种物质的性质和过程中的实验现象等方面的知识,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
3.2015年10月,我国科学家屠呦呦因发现青蒿素(化学式为C15H22O5,相对分子质量为282,一种用于治疗疟疾的药物)而获得诺贝尔生理学或医学奖.青蒿素的发现挽救了全球特别是发展中国家数百万人的生命.下列有关青蒿素的说法正确的是( )
| A. | 青蒿素属于氧化物 | |
| B. | 青蒿素中碳、氢、氧元素的质量比为15:22:5 | |
| C. | 青蒿素不属于有机化合物 | |
| D. | 青蒿素中氢元素的质量分数为7.8% |
1.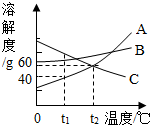 如图是A、B、C三种物质的溶解度曲线,下列说法错误的是( )
如图是A、B、C三种物质的溶解度曲线,下列说法错误的是( )
 如图是A、B、C三种物质的溶解度曲线,下列说法错误的是( )
如图是A、B、C三种物质的溶解度曲线,下列说法错误的是( )| A. | t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A | |
| B. | A可以采用冷却热饱和溶液的方法结晶 | |
| C. | t2℃时,A、C两种溶液的溶解度相等 | |
| D. | t2℃时,A、C两种溶液的溶质质量分数一定相等 |
5.实验室开放日,老师给某化学兴趣小组一包氧化铜的混合物样品,要求兴趣小组测定样品中氧化铜的质量分数.同学们称取5g样品于烧杯中,再把20g稀硫酸平均分四次加入到烧杯中并进行搅拌,让其充分反应.有关实验数据记录如下:
求:
(1)氧化铜中铜元素和氧元素的质量比为4:1.
(2)硫酸分子中各原子的个数比H:S:O=2:1:4.
(3)样品中铜的质量为3g.
(4)第4次反应后所得溶液中硫酸铜的质量分数.
| 实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 加入的稀硫酸的质量/g | 5 | 5 | 5 | 5 |
| 烧杯中剩余固体的质量/g | 4.2 | 3.4 | 3.0 | 3.0 |
(1)氧化铜中铜元素和氧元素的质量比为4:1.
(2)硫酸分子中各原子的个数比H:S:O=2:1:4.
(3)样品中铜的质量为3g.
(4)第4次反应后所得溶液中硫酸铜的质量分数.
2.如表列出了除去物质中所含少量杂质的方法,其中正确的是( )
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | NaOH | NaCl | 加入适量的稀盐酸 |
| B | FeCl2 | CuCl2 | 加入过量铁粉、充分反应后过滤 |
| C | KCl | MnO2 | 加水溶解、过滤、洗涤、干燥 |
| D | Na2SO4 | H2SO4 | 加过量的碳酸钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
