题目内容
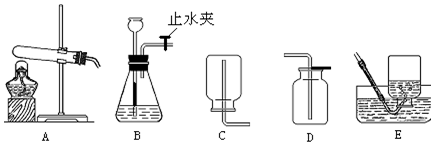
17.现有实验室制取气体的部分装置,请结合所学化学知识,回答有关问题:
(1)请填写标号仪器的名称:a试管,b分液漏斗,c集气瓶,d导管;
(2)工业制氧气属于物理变化(填物理或化学).实验室用过氧化氢溶液制取氧气,可用的发生装置是B,收集装置选用C或D,加入药品前应进行的操作是检验装置气密性,固体二氧化锰起催化作用,请写出反应的化学反应式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)若用氯酸钾制氧气,可用的发生装置是A,若用c收集,氧气收集满时,应在集气瓶口盖上,再正(填正或者倒)放在桌面上,然后先撤导管,再熄灭酒精灯.
(4)氨气是一种无色有刺激性气味、极易溶于水,密度比空气小的气体.实验室常用加热氯化铵和熟石灰的固体混合物制取氨气,则其发生装置应选择A,收集装置应选择E.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据工业制取氧气的过程中,没有新物质生成,属于物理变化,过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,氧气的密度比空气大,溶于水,加入药品前应进行的操作是:检验装置气密性,二氧化锰是该反应的催化剂,过氧化氢在二氧化锰的催化作用下分解生成水和氧气进行分析;
(3)根据氯酸钾制取氧气的反应物是固体,反应条件是加热,氧气密度比空气大,排水法收集氧气,实验结束先撤导管,再熄灭酒精灯进行分析;
(4)根据实验室制取氨气的反应物是固体,反应条件是加热,氨气极易溶于水,密度比空气小进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是试管,b是分液漏斗,c是集气瓶,d是导管;
(2)工业制取氧气的过程中,没有新物质生成,属于物理变化,过氧化氢制取氧气的反应物是固体和液体,反应条件是常温,氧气的密度比空气大,溶于水,所以可用的发生装置是B,收集装置选用C或D,加入药品前应进行的操作是:检验装置气密性,二氧化锰是该反应的催化剂,起催化作用,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)氯酸钾制取氧气的反应物是固体,反应条件是加热,所以可用的发生装置是A,氧气密度比空气大,所以用C收集,氧气收集满时,应在集气瓶口盖上玻璃片,再正放在桌面上,然后先撤导管,再熄灭酒精灯;
(4)实验室制取氨气的反应物是固体,反应条件是加热,氨气极易溶于水,密度比空气小,所以发生装置应选择A,收集装置应选择E.
故答案为:(1)试管,分液漏斗,集气瓶,导管;
(2)物理,B,C或D,检验装置气密性,催化,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)A,玻璃片,正,撤导管,熄灭酒精灯;
(4)A,E.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

| A. | Na2CO3 苏打 碳酸钠 | B. | CaO 生石灰 消石灰 | ||
| C. | Ca(OH)2熟石灰 氢氧化钙 | D. | NaOH 烧碱 苛性钠 |
| A. | 浓硫酸沾在皮肤上,用烧碱溶液处理 | |
| B. | 油锅着火时应迅速浇水熄灭 | |
| C. | 室内烤火取暖放一盆水,防止一氧化碳中毒 | |
| D. | 发现燃气泄漏应立即关闭气阀、开窗通风、严禁烟火 |
| A. |  倾倒液体 | B. |  稀释浓硫酸 | C. |  加热液体 | D. |  过滤 |