题目内容
8.目前常用的1元硬币为钢芯镀镍合金,5角硬币为铜锌合金或钢芯镀铜合金,1角硬币为铝锌合金或不锈钢,请回答下列问题:(1)铸造硬币的合金不需考虑的是D
A.耐磨性 B.抗腐蚀性 C.色泽 D.导电性
(2)硬币涉及到的金属有Al、Ni(镍)、Zn、Cu、Fe,Ni能发生如下反应:
Ni+H2SO4═NiSO4+H2↑ Fe+NiSO4═Ni+FeSO4
以上5种金属活动性由强到弱顺序是Al>Zn>Fe>Ni>Cu.
(3)Ni与AgNO3溶液能(填“能”与“不能”)反应.
(4)工业上用NiO与CO在高温下反应冶炼镍,写出反应的化学方程式CO+NiO$\frac{\underline{\;高温\;}}{\;}$Ni+CO2,这是利用了CO的还原性(填氧化性、还原性或可燃性).
分析 (1)根据铸造金币的物质的性质考虑;
(2)在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,氢前的金属能与酸反应生成氢气;
(3)根据在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来分析解答;
(4)根据用NiO与CO在高温下反应冶炼镍,利用的是一氧化碳的还原性,写出反应的方程式.
解答 解:(1)铸造硬币的合金需要具备耐磨性、抗腐蚀性好、具有一定的金属光泽,价格不易过于贵重,不需要考虑其导电性;
(2)Ni+H2SO4═NiSO4+H2↑,说明镍在氢的前面,Fe+NiSO4═Ni+FeSO4,说明铁在镍的前面,故金属的活动性顺序为:Al>Zn>Fe>Ni>Cu;
(3)镍在铜的前面,铜在银的前面,故镍的活动性强于银,能与硝酸银溶液反应;
(4)用NiO与CO在高温下反应冶炼镍,利用的是一氧化碳的还原性,反应的方程式是:CO+Ni$\frac{\underline{\;高温\;}}{\;}$Ni+CO2.
故答案为:
(1)D;(2)Al>Zn>Fe>Ni>Cu;(3)能;(4)CO+NiO$\frac{\underline{\;高温\;}}{\;}$Ni+CO2;还原性.
点评 掌握金属的性质是解答本题的关键.要熟练掌握金属活动性顺序及其意义.

练习册系列答案
相关题目
13.下列实验操作不正确的是( )
| A. | 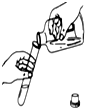 | B. |  | C. |  | D. | 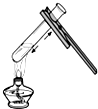 |
17.下列物质中属于纯净物的是( )
| A. | 食盐水 | B. | 冰水混合物 | C. | 天然气 | D. | 石油 |
6.能闻到花香的原因是( )
| A. | 分子的质量和体积都很小 | B. | 分子间有间隔 | ||
| C. | 分子在不断运动 | D. | 分子由原子构成 |
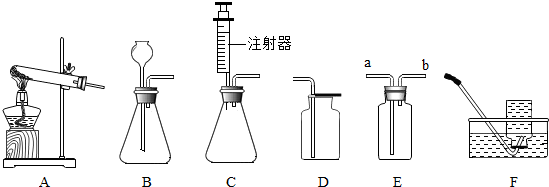
 碘元素对人体健康起着重要的作用,在食盐中加碘可有效预防甲状腺肿大的发生.如图是某品牌加碘盐的标签,请回答下列问题.
碘元素对人体健康起着重要的作用,在食盐中加碘可有效预防甲状腺肿大的发生.如图是某品牌加碘盐的标签,请回答下列问题.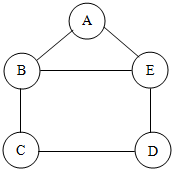 小吴用铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五中物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生反应.其中C物质的溶液呈蓝色,A与E反应产生的气体是光合作用的原料之一.
小吴用铁、硫酸、氢氧化钡、硫酸铜和碳酸钠五中物质玩化学拼图游戏(如图),游戏规则要求图中相邻物质之间能发生反应.其中C物质的溶液呈蓝色,A与E反应产生的气体是光合作用的原料之一.