题目内容
18.如图所示为实验室中常见的气体制备和收集装置.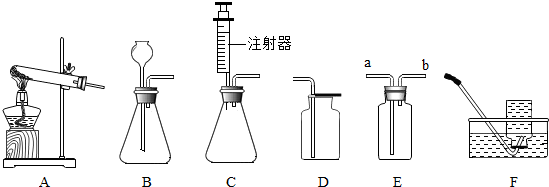
请回答下列问题:
(1)实验室用高锰酸钾制取氧气,应选用发生装置A(填字母序号),反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.若用装置D收集氧气,验满的方法是将带火星的木条放在集气瓶口,若木条复燃,证明氧气已集满.
(2)实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C做发生装置,你认为选用C的优点是能控制产生气体的速率.
(3)欲使用装置E用排空气法收集二氧化碳,则气体应从a(填“a”或“b”)端通入;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从b(填“a”或“b”)端通入.
(4)已知一氧化氮气体难溶于水,在空气中容易与氧气发生反应,则收集一氧化氮气体时应选用图中装置E(填字母序号).
分析 (1)根据实验室用高锰酸钾制取氧气,属于固体加热型制取气体,高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,氧气有助燃性进行分析;
(2)观察图形可知,C是用注射器添加液体,然后考虑注射器的优点进行分析;
(3)根据二氧化碳密度比空气大,氧气密度比水小,不易溶于水进行分析;
(4)根据气体收集方法的确定因素进行分析.
解答 解:(1)实验室用高锰酸钾制取氧气,属于固体加热型,应该选用的发生装置是A,高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,化学方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,利用氧气支持燃烧的性质,可用带火星的木条放在集气瓶口,若木条复燃证明氧气已集满;
(2)装置C滴加液体的仪器是注射器,用注射器代替长颈漏斗,可以使滴加的液体随加随停,可控制产生气体的速率;
(3)二氧化碳密度比空气大,所以用装置E用排空气法收集二氧化碳,则气体应从a端通入,氧气密度比水小,不易溶于水,所以使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从b端通入;
(4)已知一氧化氮气体难溶于水,可选用排水法收集;在空气中容易与氧气发生反应,不能选用排空气法收集,所以收集一氧化氮气体时应选用排水法收集.
故答案为:(1)A,2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,用带火星的木条放在集气瓶口,若木条复燃证明氧气已集满;
(2)能控制产生气体的速率;
(3)a,b;
(4)E.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
相关题目
8.分类是学习和研究化学的常用方法.下列分类中正确的是( )
| A. | 有机物 甲烷 乙醇 葡萄糖 | |
| B. | 复合肥料 尿素 硝酸钾 磷酸二氢铵 | |
| C. | 合成材料 合金 合成纤维 合成橡胶 | |
| D. | 混合物 煤 石油 冰水共存物 |
6.下列试剂中,能把BaCl2、KOH、H2SO4三种溶液一次性鉴别出来的是( )
| A. | NH4NO3溶液 | B. | Na2 SO4溶液 | C. | K2CO3溶液 | D. | FeCl3溶液 |
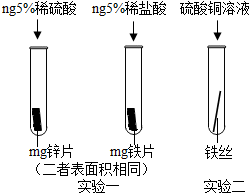 铁元素与人类的关系密切.
铁元素与人类的关系密切.