题目内容
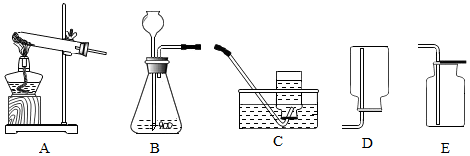
11.小明用加热氯酸钾和二氧化锰混合物的方法制氧气,现取15克干燥的氯酸钾和2克二氧化锰混合物放入试管中加热,收集了所需的氧气后,停止加热让试管冷却,称得试管内剩余固体的质量为12.2克.(1)发生的化学反应方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(2)得到的氧气质量是4.8g;
(3)试管内剩余固体中有氯酸钾、氯化钾和二氧化锰物质(填化学式),计算剩余固体各物质的质量分别是多少?
分析 氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,反应前后的质量差即为反应生成氧气的质量,根据反应的化学方程式及其提供的数据可以进行相关方面的计算和判断.
解答 解:(1)氯酸钾在二氧化锰催化作用下受热分解生成氯化钾和氧气,发生的化学反应方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
故填:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(2)得到的氧气质量是:15g+2g-12.2g=4.8g,
故填:4.8g.
(3)设反应的氯酸钾质量为x,生成氯化钾质量为y,
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,
245 149 96
x y 4.8g
$\frac{245}{x}$=$\frac{149}{y}$═$\frac{96}{4.8g}$,
x=12.25g,y=7.45g,
试管内剩余固体中有氯酸钾、氯化钾和二氧化锰,氯酸钾质量为:15g-12.25g=2.75g,
即试管内剩余固体中有氯酸钾、氯化钾和二氧化锰的质量分别是2.75g、7.45g、2g.
故填:氯酸钾、氯化钾和二氧化锰;
答:剩余固体中氯酸钾、氯化钾和二氧化锰的质量分别是2.75g、7.45g、2g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
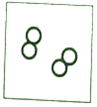
1.如图是某化学反应的微观示意图,下列说法错误的是( )


| A. | 反应前和反应后的物质均为混合物 | |
| B. | 参加反应的分子个数比为3:2 | |
| C. | 反应前后原子的种类、数目不变 | |
| D. | 生成物中含有碳元素、氢元素和氧元素 |
20.下列实验方案能够达到目的是( )
| 选项 | 实验内容 | 实验方案 |
| A | 鉴别碳酸钠和大理石粉 | 分别向两种粉末中滴加稀盐酸 |
| B | 鉴别稀盐酸和稀硫酸 | 分别向两种溶液中滴加氯化钡溶液 |
| C | 除去二氧化碳中的水蒸气和氯化氢气体 | 将气体先通过足量氢氧化钠溶液,再通过浓硫酸 |
| D | 除去铁粉中的少量碳粉 | 在空气中加热 |
| A. | A | B. | B | C. | C | D. | D |