题目内容
3.下列离子可在同一溶液中大量共存的是( )| A. | SO42- H+ Na+ OH- | B. | Cl- K+ Ca2+ NO3- | ||
| C. | H+ SO42- K+ CO32- | D. | Ca2+ CO32- NO3- Na+ |
分析 根据离子之间不能结合生成水、气体、沉淀、弱电解质等,则离子能大量共存,以此来解答.
解答 解:A、H+、OH-两种离子能结合成水,不能大量共存.故选项错误;
B、四种离子间不能结合成沉淀、气体或水,能大量共存,故选项正确;
C、CO32-、H+能结合生成水和二氧化碳,则不能共存,故选项错误;
D、Ca2+和CO32-结合生成碳酸钙沉淀,则不能共存,故选项错误;
故答案为:B.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.下列事实的解释正确的是( )
| A. | 铝制品经久耐用--铝比较不活泼 | |
| B. | 消防员喷水灭水的原理--隔绝空气 | |
| C. | CaO可作食品干燥剂--CaO有很强的吸水性 | |
| D. | 绿色植物光合作用吸收太阳能--太阳能转化为热能 |
11.下列有关推理的说法中正确的是( )
| A. | 蜡烛燃烧生成CO2和H2O,则蜡烛组成里一定含有碳和氢元素 | |
| B. | 氧化物含有氧元素,则含氧元素的化合物都是氧化物 | |
| C. | 碱溶液呈碱性,则呈碱性的溶液一定都是碱溶液 | |
| D. | 使用石油、煤和天然气会排放大量二氧化碳,因此要禁止开发化石能源 |
8. 请完成下列相关内容:
请完成下列相关内容:
Ⅰ.实验表明,大多数金属都能与氧气发生反应,但反应的难易和剧烈程度是不同的.
(1)铁在潮湿的空气中易生锈,铁锈的主要成分为Fe2O3•ⅹH2O(或Fe2O3);铁在氧气中能剧烈燃
烧,现象为剧烈燃烧,火星四射,有黑色固体生成,反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(2)铜在潮湿的空气中也容易锈蚀生成铜绿,其主要成分是碱式碳酸铜[Cu2(OH)2CO3],铜锈蚀除了与氧气有关外,还与空气中的水和二氧化碳有关.
(3)铝在空气中具有很好的抗腐蚀性能,其原因是铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化.
Ⅱ.过氧化钠(Na2O2)是一种淡黄色固体,能与水或二氧化碳反应放出氧气.实验室有一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分.
【提出问题】变质的过氧化钠粉末中有哪些成分?
【查阅资料】2Na2O2+2H2O═4NaOH+O2↑
2Na2O2+2CO2═2Na2CO3+O2
【猜想与假设】(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是Na2O2和Na2CO3的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物
…
【实验探究】
【得出结论】同学们经过实验和计算分析,该固体样品中所含物质有Na2O2、NaOH和Na2CO3.
【拓展应用】过氧化钠(Na2O2)是供氧设备中常用的供氧剂.若将15.6g过氧化钠与足量的二氧化碳充分反应,理论上生成的氧气质量是多少?(写出计算过程).
 请完成下列相关内容:
请完成下列相关内容:Ⅰ.实验表明,大多数金属都能与氧气发生反应,但反应的难易和剧烈程度是不同的.
(1)铁在潮湿的空气中易生锈,铁锈的主要成分为Fe2O3•ⅹH2O(或Fe2O3);铁在氧气中能剧烈燃
烧,现象为剧烈燃烧,火星四射,有黑色固体生成,反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(2)铜在潮湿的空气中也容易锈蚀生成铜绿,其主要成分是碱式碳酸铜[Cu2(OH)2CO3],铜锈蚀除了与氧气有关外,还与空气中的水和二氧化碳有关.
(3)铝在空气中具有很好的抗腐蚀性能,其原因是铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化.
Ⅱ.过氧化钠(Na2O2)是一种淡黄色固体,能与水或二氧化碳反应放出氧气.实验室有一瓶放置了较长时间的过氧化钠粉末,已知发生了部分变质,同学们取3.00g变质粉末决定探究其中的成分.
【提出问题】变质的过氧化钠粉末中有哪些成分?
【查阅资料】2Na2O2+2H2O═4NaOH+O2↑
2Na2O2+2CO2═2Na2CO3+O2
【猜想与假设】(1)粉末成分是Na2O2和NaOH的混合物
(2)粉末成分是Na2O2和Na2CO3的混合物
(3)粉末成分是Na2O2、NaOH 和Na2CO3的混合物
…
【实验探究】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取3.00g变质粉末于一支大试管中,加入适量的水,共收集到0.32g气体,然后用带火星木条检验生成的气体. | 固体完全溶解, 带火星的木条复燃 | 该固体样品中含有Na2O2,其质量为1.56g. |
| ②继续向上述试管中加入足量的石灰水,充分反应. | 有白色沉淀 | 化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH. |
| ③将②中物质过滤,得到滤渣,将其洗涤、干燥并称量,得固体1.00g. | / | / |
【拓展应用】过氧化钠(Na2O2)是供氧设备中常用的供氧剂.若将15.6g过氧化钠与足量的二氧化碳充分反应,理论上生成的氧气质量是多少?(写出计算过程).
15.下列实验设计不能达到实验目的是( )
| A. | 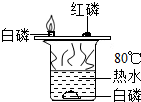 验证可燃物燃烧的条件 | |
| B. | 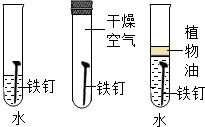 探究铁生锈的条件 | |
| C. | 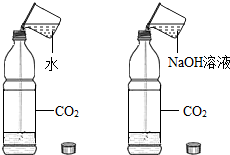 证明CO2和NaOH反应 | |
| D. | 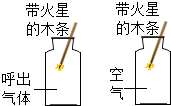 探究呼出气体和空气中氧气含量的不同 |
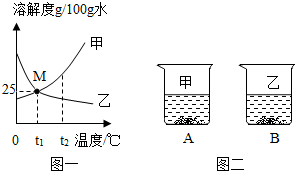 图一为甲、乙两种物质(不带结晶水)的溶解度曲线图.
图一为甲、乙两种物质(不带结晶水)的溶解度曲线图.