题目内容
4.在一个密闭容器中放入X,Y,Z,W四种物质,在一定条件下发生化学反应,一段时间后,测得相关数据如表,下列关于此反应的认识,正确的是( )| 物 质 | X | Y | Z | W |
| 反应前的质量/g | 10 | m | 8 | 7 |
| 反应后的质量/g | 2 | 3 | 30 | 25 |
| A. | m的数值为32 | |
| B. | 参加反应的X与Y的质量比为1:4 | |
| C. | 若W为水,则X或Y必定为酸或碱 | |
| D. | 若X为化合物,Y为单质,则Z和W中也一定有一种单质 |
分析 本题可分析先X、Z、W三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定m的值,推测Y是反应物还是生成物,进而进行分析.
解答 解:由表中数据分析可知,反应前后X的质量减少了10g-2g=8g,故X是反应物,参加反应的X的质量为8g;同理可以确定Z是生成物,生成的Z的质量为30g-8g=22g;W是生成物,生成的W的质量为25g-7g=18g;由质量守恒定律,Y应是反应物,且参加反应的Y的质量为22g+18g-8g=32g,故该反应为:X+Y→Z+W.
A、由质量守恒定律,Y应是反应物,且参加反应的Y的质量为22g+18g-8g=32g,故m的数值为3g+32g=35g,故选项说法错误.
B、参加反应的X与Y的质量比为8g:32g=1:4,故选项说法正确.
C、该反应的反应物为X和Y,生成物是W和Z,若W为水,由于无法确定X、Y的元素组成,X或Y不一定为酸或碱,如甲烷燃烧也能生成水,但反应物不是酸或碱,故选项说法错误.
D、X、Y是反应物,Z和W是生成物,若X为化合物,Y为单质,无法确定Z和W中是否是单质;故选项说法错误.
故选:B.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中化合价不发生变化.常温下,MFe2Ox能使工业废气中的SO2转化为S,转化流程如图所示:
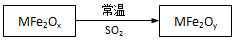
已知MFe2Oy中Fe为+3价.下列说法中,正确的是( )

已知MFe2Oy中Fe为+3价.下列说法中,正确的是( )
| A. | y的数值为5 | B. | SO2不是该反应的催化剂 | ||
| C. | MFe2Ox发生了分解反应 | D. | 该过程是物理变化 |
7.比较、推理是化学学习常用的方法,以下是根据一些反应事实推导出的影响化学反应的因素,其中推理不合理的是( )
| 序号 | 化学反应事实 | 影响化学反应的因素 |
| A | 铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 | 反应物浓度 |
| B | 水要在通电的条件才能分解,而双氧水只要加入二氧化锰就迅速分解 | 催化剂 |
| C | 碳在常温下不与氧气发生反应,而在高温时能与氧气反应 | 反应温度 |
| D | 铜片在空气中很难燃烧,钠米铜粉在空气中较易燃烧 | 反应物的接触面积 |
| A. | A | B. | B | C. | C | D. | D |
14.25℃时,某气态碳氢化合物与氧气混合后装入密闭容器中,经充分反应后,又恢复25℃,此时容器内气体分子是反应前的一半.再经足量的氢氧化钠溶液吸收后,容器内几乎成真空.此碳氢化合物可能是( )(本题不考虑生成一氧化碳)
| A. | CH4 | B. | C2H6 | C. | C2H2 | D. | C3H8 |
9.除去下列物质中的杂质所加试剂及所用方法均不正确的是( )
| 物质(括号内为杂质) | 试剂 | 除去杂质的方法 | |
| A | NaCl溶液(NaHCO3) | 过量稀盐酸 | 蒸发 |
| B | FeSO4 溶液(CuSO4) | 过量铁粉 | 过滤 |
| C | O2 (CO2) | 足量氢氧化钠溶液 | 洗气 |
| D | BaCO3(BaSO4) | 稀硫酸 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
16.某同学做了如下图所示实验并对实验数据和现象记录如下表,请回答下列问题: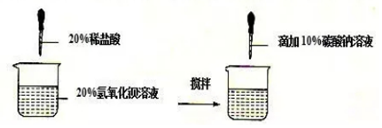
(1)写出第一次实验中加入盐酸后发生反应的化学方程式2HCl+Ba(OH)2═BaCl2+2H2O.
(2)第一次实验结束后所得溶液中溶质的化学式为NaCl和NaOH.
(3)根据已知条件求解出第二次实验生成白色沉淀X的比例式$\frac{106}{21.2g}=\frac{197}{X}$.
(4)第二次实验中每一步所加物质均恰好完全反应
(5)若向第二次的溶液中加入51.4g水,则所得不饱和溶液中溶质的质量分数为5%.
(6)若配制实验中需要的稀盐酸,需用36.5%的浓盐酸的质量为140g.

| 实验次数 | 第一次 | 第二次 | 第三次 |
| 氢氧化钡溶液质量 | 171g | 171g | 171g |
| 滴加盐酸的质量 | 36.5g | 73g | 146g |
| 滴加碳酸钠溶液质量 | 212g | 212g | 212g |
(2)第一次实验结束后所得溶液中溶质的化学式为NaCl和NaOH.
(3)根据已知条件求解出第二次实验生成白色沉淀X的比例式$\frac{106}{21.2g}=\frac{197}{X}$.
(4)第二次实验中每一步所加物质均恰好完全反应
(5)若向第二次的溶液中加入51.4g水,则所得不饱和溶液中溶质的质量分数为5%.
(6)若配制实验中需要的稀盐酸,需用36.5%的浓盐酸的质量为140g.
13.翡翠,是硬玉的一种,主要成分为NaAlSi2O6,是生活中常见的一种饰品和收藏品.下列有关翡翠主要成分的说法不正确的是( )
| A. | 该物质是由四种元素组成 | |
| B. | 该物质属于化合物 | |
| C. | 该物质中钠、铝、硅、氧原子个数比为1:1:2:6 | |
| D. | 该物质中Si元素化合价为+3价 |
14.鉴别下列物品方法不正确的是( )
| 选项 | 鉴别的物质 | 鉴别的方法 |
| A | 冰和干冰 | 室温(20℃)放置,过一段观察是否有水渍 |
| B | 水和双氧水 | 加二氧化锰,观察是否有气泡 |
| C | 二氧化锰和氧化铜 | 观察颜色 |
| D | 纯羊毛和化纤面料 | 灼烧闻气味 |
| A. | A | B. | B | C. | C | D. | D |