题目内容
9.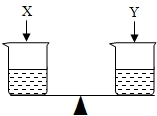 如图在天平两边的烧杯中分别盛有等质量、等质量分数的足量的稀硫酸,然后向左、右两边分别加入X、Y两种等质量的金属,发现天平的指针先偏向右边,最后偏向左边,则X、Y可能是( )
如图在天平两边的烧杯中分别盛有等质量、等质量分数的足量的稀硫酸,然后向左、右两边分别加入X、Y两种等质量的金属,发现天平的指针先偏向右边,最后偏向左边,则X、Y可能是( )| A | B | C | D |
| X:Mg | X:Fe | X:Cu | X:Mg |
| Y:Al | Y:Zn | Y:Fe | Y:Fe |
| A. | A | B. | B | C. | C | D. | D |
分析 烧杯中的硫酸足量,因此反应产生氢气的多少决定于金属的质量;金属与酸反应放出氢气,使天平两端质量减小,但由于金属活动性不同与酸反应放出氢气的速度也不同,天平两端质量减少的速率也不同;由于等质量的金属完全反应放出氢气质量不同,因此,两端金属完全反应后天平仍不能平衡;因此,需要根据天平指针的偏向,确定金属的活动性及等质量金属完全反应放出氢气质量的大小,判断两种金属.
解答 解:天平的指针先偏向右边,说明天平左边质量减少地较慢,即右边金属与酸反应比左边反应剧烈,右边金属活动性比左边的活动性强;金属Mg、Al、Fe、Zn的活动性从强到弱的顺序为:Mg>Al>Zn>Fe;最后偏向左边,说明到反应结束时右边产生气体较少即等质量金属完全反应右边产生氢气的量小于左边;等质量的Mg、Al、Fe、Zn与足量的酸完全反应产生氢气质量从大到小的顺序为:Al>Mg>Fe>Zn;
A、Mg的活动性比Al强,不符合右边金属活动性比左边的活动性强,故A错误;
B、Zn的活动性比铁强,根据氢气质量=$\frac{金属的化合价}{金属的相对原子质量}$×金属质量,所以同质量的Fe、Zn是铁生成的氢气多,所以符合实验现象的情况,故B正确;
C、铜不会与稀硫酸反应、天平始终是偏向左边的,故C错误;
D、Mg的活动性比Zn强,不符合右边金属活动性比左边的活动性强,故D错误.
故选:B.
点评 本题考查了金属与酸反应的速度和产生的氢气质量关系,完成此题,要根据金属活动性顺序的意义和金属与酸反应生成氢气的质量规律进行.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
19.如图的反应中,甲、乙、丙三种分子的个数比为1:3:2,则从图示中获得的信息正确是( )


| A. | 该反应中元素化合价一定改变 | B. | 原子种类在化学反应中发生了变化 | ||
| C. | 生成物一定属于氧化物 | D. | 乙分子中A与B的原子个数比为1:2 |
20.关于一氧化碳和二氧化碳的叙述正确的是( )
| A. | 一氧化碳和二氧化碳均有可燃性 | |
| B. | 室内放一盆水能防止一氧化碳中毒 | |
| C. | 一氧化碳具有还原性可用于冶炼金属 | |
| D. | 可用氢氧化钠来溶液鉴别某气体是否是二氧化碳 |
 小童将观察到的现象形象地画了一幅卡通画,每个卡通人物表示一种金属,周围的小黑点表示反应中生成的气体.如图所示:
小童将观察到的现象形象地画了一幅卡通画,每个卡通人物表示一种金属,周围的小黑点表示反应中生成的气体.如图所示: