题目内容
1.如图1是实验室常用的一些装置: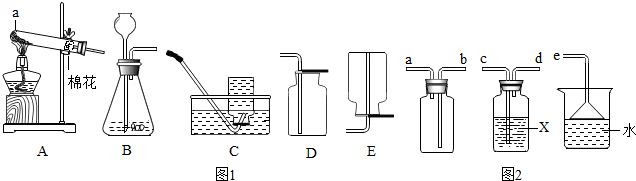
(1)仪器a的名称:试管;
(2)实验室制取并收集二氧化碳气体应选择的装置是BD(填序号),检验二氧化碳是否收集满的方法是把燃着的木条放在集气瓶口,如果熄灭,证明集气瓶内已充满二氧化碳;
(3)用装置A与C连接制取并收集氧气,则装置A中反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,当观察到装置C中导管口气泡连续、均匀冒出时才开始收集;
(4)SO2通常是一种无色有刺激性气味的有毒气体,密度比空气大,易溶于水,排放到空气中会形成酸雨,实验室用如图2装置收集一瓶干燥的SO2,装置的导管按气流方向连接的顺序是c→d→b→a→e(填字母),装置中的X是浓硫酸.
分析 (1)熟记仪器的名称;
(2)从实验室制二氧化碳的反应条件是不需要加热,故发生装置为B,二氧化碳气体的密度比空气大、能溶于水,故只能用向上排空气法而不能用排水法,由于二氧化碳的密度比空气大,进入集气瓶后,沉积在集气瓶的底部,二氧化碳自下而上,充满集气瓶,当瓶口有二氧化碳时,说明二氧化碳已收集满去分析解答;
(3)A装置是用加热固体的方法制取氧气,且试管口有棉花,说明是用加热高锰酸钾的方法制取氧气,据反应原理书写方程式,利用排水法收集气体时,要等导管口气泡连续、均匀冒出时再开始收集,防止收集的气体不纯;
(4)实验室用如图2装置收集一瓶干燥的SO2,装置的导管按气流方向连接的顺序是长进短出,因此是c进d出,装置中的X是浓硫酸起干燥作用;然后b进a出,因为二氧化硫的密度比空气大.
解答 解:(1)仪器a是试管;故填:试管;
(2)大理石(主要成分是CaCO3)和稀盐酸(主要成分HCl),二者接触即可发生反应生成氯化钙、水和二氧化碳,由于实验室制二氧化碳的反应条件是不需要加热,故发生装置为B,二氧化碳气体的密度比空气大、能溶于水,故只能用向上排空气法而不能用排水法,故收集装置为D;由于二氧化碳的密度比空气大,进入集气瓶后,沉积在集气瓶的底部,二氧化碳自下而上,充满集气瓶,当瓶口有二氧化碳时,说明二氧化碳已收集满;由于二氧化碳不能支持燃烧,所以把燃着的木条放在集气瓶口,如果熄灭,证明集气瓶内已充满二氧化碳;故答案为:BD;把燃着的木条放在集气瓶口,如果熄灭,证明集气瓶内已充满二氧化碳.
(3)A装置是用加热固体的方法制取氧气,且试管口有棉花,说明是用加热高锰酸钾的方法制取氧气,方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,利用排水法收集气体时,要等导管口气泡连续、均匀冒出时再开始收集,防止收集的气体不纯;故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;导管口气泡连续、均匀冒出;
(4)实验室用如图2装置收集一瓶干燥的SO2,装置的导管按气流方向连接的顺序是长进短出,因此是c进d出,装置中的X是浓硫酸起干燥作用;然后b进a出,因为二氧化硫的密度比空气大;故答案为:c;d;b;a;浓硫酸.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的干燥等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 应用题作业本系列答案
应用题作业本系列答案| A. | 7.2g | B. | 6.0g | C. | 9.6g | D. | 8.0g |
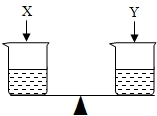 如图在天平两边的烧杯中分别盛有等质量、等质量分数的足量的稀硫酸,然后向左、右两边分别加入X、Y两种等质量的金属,发现天平的指针先偏向右边,最后偏向左边,则X、Y可能是( )
如图在天平两边的烧杯中分别盛有等质量、等质量分数的足量的稀硫酸,然后向左、右两边分别加入X、Y两种等质量的金属,发现天平的指针先偏向右边,最后偏向左边,则X、Y可能是( )| A | B | C | D |
| X:Mg | X:Fe | X:Cu | X:Mg |
| Y:Al | Y:Zn | Y:Fe | Y:Fe |
| A. | A | B. | B | C. | C | D. | D |
| 物质 | 白磷 | 红磷 | 木材 | 酒精 |
| 着火点/℃ | 40 | 240 | 250~300 | 558 |
| A. | 红磷燃烧属于化合反应 | |
| B. | 实验时,用于吸干白磷的滤纸片不能丢在废纸篓里 | |
| C. | 白磷、红磷、木材、酒精都是可燃物 | |
| D. | 降低可燃物的着火点可以达到灭火的目的 |
 要使如图装置中的小气球明显鼓起来,则使用的固体和液体可以是( )
要使如图装置中的小气球明显鼓起来,则使用的固体和液体可以是( )①锌和稀硫酸 ②石灰石和稀盐酸
③蔗糖和水 ④硝酸铵和水.
| A. | ①② | B. | ①②③ | C. | ①②④ | D. | ①②③④ |
| A. | pH<5.6的雨水称为酸雨 | |
| B. | 使用乙醇汽油能减少污染,节约石油资源 | |
| C. | “温室效应”主要是由CO2等气体引起的 | |
| D. | 煤、石油、天然气、风能是人类正在开发使用的新能源 |