题目内容
4.A~G是初中化学常见的物质,其中E为黑色固体.如图为这些物质的转化关系图,其中部分生成物和反应条件已省略.
(1)A的化学式为CaCO3.
(2)①②③④⑤⑥中,属于化合反应的是②(填序号,下同),属于复分解反应的是 ④⑤⑥.
(3)⑥的化学方程式为CuSO4+2NaOH═Na2SO4+Cu(OH)2↓.
(4)⑤的化学方程式为CuO+H2SO4═CuSO4+H2O,反应的现象是黑色固体逐渐溶解,溶液由无色变成蓝色.
分析 根据A-G是初中常见的物质,E是黑色固体,能与硫酸反应生成G,且G能与F反应生成蓝色沉淀,则G是硫酸铜,F是氢氧化钠,E是氧化铜,氧化铜能与一氧化碳反应生成C,则C可能是二氧化碳,A能高温反应生成B和二氧化碳,则A是碳酸钙,B是氧化钙,氧化钙能与水反应生成氢氧化钙,然后将推出的物质进行验证即可.
解答 解:(1)A-G是初中常见的物质,E是黑色固体,能与硫酸反应生成G,且G能与F反应生成蓝色沉淀,则G是硫酸铜,F是氢氧化钠,E是氧化铜,氧化铜能与一氧化碳反应生成C,则C可能是二氧化碳,A能高温反应生成B和二氧化碳,则A是碳酸钙,B是氧化钙,氧化钙能与水反应生成氢氧化钙,经过验证,推导正确,所以A是CaCO3;
(2)①是碳酸钙高温分解,属于分解反应,②是氧化钙和水的反应,属于化合反应,③是氧化铜和一氧化碳的反应,不属于反应基本类型,④是氢氧化钙和碳酸钠的反应,属于复分解反应,⑤是氧化铜和硫酸的反应,属于复分解反应,⑥是氢氧化钠和硫酸铜的反应,属于复分解反应,所以属于化合反应的是②,属于复分解反应的是④⑤⑥;
(3)⑥是氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:CuSO4+2NaOH═Na2SO4+Cu(OH)2↓;
(4)⑤是氧化铜和硫酸反应生成硫酸铜和水,化学方程式为:CuO+H2SO4═CuSO4+H2O,实验现象为:黑色固体逐渐溶解,溶液由无色变成蓝色.
故答案为:(1)CaCO3;
(2)②,④⑤⑥;
(3)CuSO4+2NaOH═Na2SO4+Cu(OH)2↓;
(4)CuO+H2SO4═CuSO4+H2O,黑色固体逐渐溶解,溶液由无色变成蓝色.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 金钥匙试卷系列答案
金钥匙试卷系列答案 铁、氯化铜、石灰水、稀盐酸、石灰石之间的反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的类型或主要实验现象.下列说法中错误的是( )
铁、氯化铜、石灰水、稀盐酸、石灰石之间的反应关系如图所示,图中两圆相交部分(a、b、c、d)表示物质间反应的类型或主要实验现象.下列说法中错误的是( )| A. | a处产生黑色物质 | B. | b处生成蓝色沉淀 | ||
| C. | c处发生复分解反应 | D. | d处产生气泡 |
| A. | 金属材料 | B. | 复合材料 | C. | 有机高分子材料 | D. | 无机非金属材料 |
| A. | 水能灭火,所以电器着火应立即用水浇灭 | |
| B. | 镁条在空气中燃烧后的固体质量大于镁条的质量,所以该反应不符合质量守恒定律 | |
| C. | 酸和碱能发生中和反应,故硝酸与氢氧化钠也能发生中和反应 | |
| D. | 碳酸盐能与稀盐酸反应放出气体,故能与稀盐酸反应放出气体的物质一定是碳酸盐 |
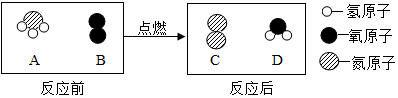
| A. | A中各元素的质量比为14:1 | B. | A中氮元素的化合价为+3 | ||
| C. | 该反应中B和C的质量比为12:7 | D. | 该反应中A和D 的分子个数比为1:1 |
| A. |  稀释10%NaOH和10% H2SO4 | |
| B. |  向等量的稀硫酸中分别逐渐加入足量的锌粉和铁粉 | |
| C. |  将水通电电解一段时间 | |
| D. |  加热一定量高锰酸钾固体 |
