题目内容
8.用化学方程式表示除去下列各物质中杂质的原理(括号内的物质为杂质)(1)KCl(K2CO3)K2CO3+2HCl═2KCl+H2O+CO2↑;
(2)CO(CO2)CO2+2NaOH═Na2CO3+H2O;
(3)金属铜(金属锌)Zn+2HCl=ZnCl2+H2↑(合理即可).
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:(1)要除去KCl溶液中的K2CO3,实质就是除去碳酸根离子,可利用K2CO3溶液与适量的稀盐酸反应生成氯化钾、水和二氧化碳,至不再产生气泡为止,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:K2CO3+2HCl═2KCl+H2O+CO2↑.
(2)CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
(3)根据金属活动性顺序,锌能和酸反应,铜和酸不反应,故可用盐酸(或稀硫酸)除去锌,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Zn+2HCl=ZnCl2+H2↑(合理即可).
故答案为:(1)K2CO3+2HCl═2KCl+H2O+CO2↑;(2)CO2+2NaOH═Na2CO3+H2O;(3)Zn+2HCl=ZnCl2+H2↑(合理即可).
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
19.安多夫是一种嫩肉粉,成分是碳酸氢钠和氯化钠,小明发现将拌了安多夫粉的肉类放到锅中加入食醋等调料烧煮时会产生大量的气体,他对此颇感兴趣,决定对其进行探究.

【查阅资料】
(1)碳酸氢钠是白色细小晶体,加热到50℃以上开始逐渐分解生成碳酸钠、二氧化碳和水,440℃时完全分解.
(2)白色无水硫酸铜遇到水会变成蓝色.
【实验探究一】对烧煮时产生大量气体的探究
(1)小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2.
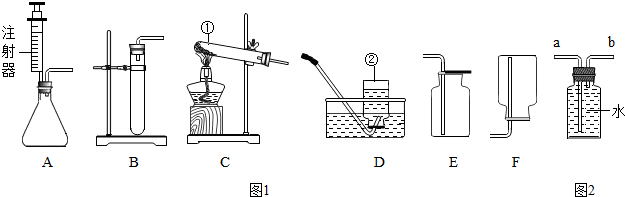
他设法收集了除去醋酸气体的气体样品,用如图1装置验证水蒸气和CO2存在.装置导气管口正确的连接顺序是为:
气体样品→d→c→b→a.
(2)小明对二氧化碳的来源作了两种猜测:
猜测①:二氧化碳可能是由碳酸氢钠与食醋中的醋酸反应产生的.
猜测②:二氧化碳可能是由碳酸氢钠受热分解产生的.
针对以上猜测,小明设计了以下实验:
【实验结论】:猜想①、②都正确
【实验探究二】测定安多夫样品中碳酸氢钠的含量
上述实验2中,小明发现充分反应后,试管中仍留有一些白色固体粉末,通过查阅资料
发现是碳酸钠和氯化钠.小明想用测定白色固体中碳酸钠的质量来推算安多夫样品中碳酸氢钠的含量,于是称取实验2中得到的白色固体粉末6.9g,设计了如图2实验方案:
(1)“操作1”中玻璃棒的作用是引流.
(2)实验中加入过量氯化钙溶液的目的是使碳酸钠完全反应.
(3)确定沉淀A已洗涤干净的方法是取最后一次洗涤液,滴加硝酸银(或碳酸钠)溶液,无沉淀产生.
(4)该安多夫样品中NaHCO3的质量分数是84%.

【查阅资料】
(1)碳酸氢钠是白色细小晶体,加热到50℃以上开始逐渐分解生成碳酸钠、二氧化碳和水,440℃时完全分解.
(2)白色无水硫酸铜遇到水会变成蓝色.
【实验探究一】对烧煮时产生大量气体的探究
(1)小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2.
他设法收集了除去醋酸气体的气体样品,用如图1装置验证水蒸气和CO2存在.装置导气管口正确的连接顺序是为:
气体样品→d→c→b→a.
(2)小明对二氧化碳的来源作了两种猜测:
猜测①:二氧化碳可能是由碳酸氢钠与食醋中的醋酸反应产生的.
猜测②:二氧化碳可能是由碳酸氢钠受热分解产生的.
针对以上猜测,小明设计了以下实验:
| 实验步骤 | 实验现象 | |
| 实验1 | 取样与试管中,加入食醋,并将产生气体通入澄清石灰水中 | 有气泡产生,石灰水变浑浊 |
| 实验2 | 取安多夫样品少许加入试管中,加热使之充分反应,并把产生的气体通入澄清石灰水 | 试管口出现小水珠,澄清石灰水变浑浊,试管中残留白色固体粉末 |
【实验探究二】测定安多夫样品中碳酸氢钠的含量
上述实验2中,小明发现充分反应后,试管中仍留有一些白色固体粉末,通过查阅资料
发现是碳酸钠和氯化钠.小明想用测定白色固体中碳酸钠的质量来推算安多夫样品中碳酸氢钠的含量,于是称取实验2中得到的白色固体粉末6.9g,设计了如图2实验方案:
(1)“操作1”中玻璃棒的作用是引流.
(2)实验中加入过量氯化钙溶液的目的是使碳酸钠完全反应.
(3)确定沉淀A已洗涤干净的方法是取最后一次洗涤液,滴加硝酸银(或碳酸钠)溶液,无沉淀产生.
(4)该安多夫样品中NaHCO3的质量分数是84%.
16.下列厨房中的物品不易溶于水的是( )
| A. | 酱油 | B. | 食盐 | C. | 花生油 | D. | 蔗糖 |
18.空气中含量最高的元素是( )
| A. | N | B. | O | C. | H | D. | C |
 现有氯化钠和碳酸钠的固体混合物19.9g,将该固体混合物完全溶解于100g水中,再向其中加入稀盐酸,生成气体质量与所加稀盐酸的质量关系如图所示.
现有氯化钠和碳酸钠的固体混合物19.9g,将该固体混合物完全溶解于100g水中,再向其中加入稀盐酸,生成气体质量与所加稀盐酸的质量关系如图所示.