题目内容
17.已知一个碳12原子的质量为1.993×10-26kg,而一个氧原子质量为2.657×10-26kg,镁原子的相对原子质量为24,求(1)该氧原子的相对原子质量.(结果保留1位小数)(2)一个镁原子的实际质量.(结果保留4位有效数字)
分析 根据某原子的相对原子质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$,结合题意进行分析解答即可.
解答 解:(1)一个碳12原子的质量为1.993×10-26kg,而一个氧原子质量为2.657×10-26kg,则该氧原子的相对原子质量为$\frac{2.657×1{0}^{-26}kg}{1.993×1{0}^{-26}kg×\frac{1}{12}}$≈16.0.
(2)一个碳12原子的质量为1.993×10-26kg,镁原子的相对原子质量为24,设一个镁原子的实际质量为x,则$\frac{x}{1.993×1{0}^{-26}kg×\frac{1}{12}}$=24,x=3.986×10-26kg.
答:(1)该氧原子的相对原子质量为16.0;(2)一个镁原子的实际质量为3.986×10-26kg.
点评 本题难度不大,掌握原子的相对原子质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$并能灵活运用是正确解答本题的关键.

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
7.中央电视台公布的我国重点城市空气质量日报的指标中不包含( )
| A. | 一氧化碳 | B. | 二氧化碳 | C. | 二氧化氮 | D. | 可吸入悬浮物 |
5.用下列装置(如图1)测定碱式碳酸镁的化学组成,计算xMgCO3•yMg(OH)2•zH2O中x:y:z的最简比.(假设每步反应、吸收均完全)
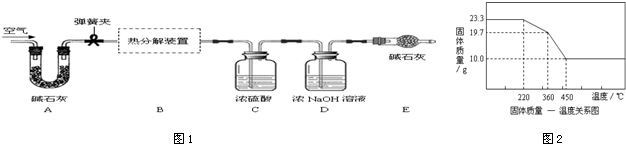
【实验步骤】
①连接好装置,检查装置的气密性;
②在热分解装置中装入23.3g样品,通人空气一段时间;
③分别称量装置C、D的质量;
④打开弹簧夹,启动热分解装置,使样品充分热解;
⑤停止加热,继续通空气至装置冷却到室温;
⑥再次分别称量装置C、D的质量.
【进行实验】该小组同学按上述实验步骤进行实验,并记录了如下数据:
【实验分析及数据处理】:
(1)A装置的作用是吸收空气中的二氧化碳和水;E装置的作用是防止空气中的二氧化碳和水进入影响实验结果;
(2)实验步骤⑤继续通空气至装置冷却到室温是为了防止热的生成物与空气中的物质反应.
(3)根据上述数据,计算xMgCO3•yMg(OH)2•zH2O中x:y:z的最简比;
(提示:MgCO3═MgO+CO2↑、Mg(OH)2═MgO+H2O)
(4)根据上述实验结论,结合“固体质量-温度关系图”(如图2),回答下列问题:
①当温度达360℃时,固体质量减少了3.6g,此质量是生成的水的质量;
②反应完全进行时,温度最低为360℃,此时热分解装置中的剩余固体物质为碳酸镁和氢氧化镁.

【实验步骤】
①连接好装置,检查装置的气密性;
②在热分解装置中装入23.3g样品,通人空气一段时间;
③分别称量装置C、D的质量;
④打开弹簧夹,启动热分解装置,使样品充分热解;
⑤停止加热,继续通空气至装置冷却到室温;
⑥再次分别称量装置C、D的质量.
【进行实验】该小组同学按上述实验步骤进行实验,并记录了如下数据:
| 装置C的质量(/g) | 装置D的质量(/g) | |
| 实验前 | 232.4 | 208.2 |
| 实验后 | 236.9 | 217.0 |
(1)A装置的作用是吸收空气中的二氧化碳和水;E装置的作用是防止空气中的二氧化碳和水进入影响实验结果;
(2)实验步骤⑤继续通空气至装置冷却到室温是为了防止热的生成物与空气中的物质反应.
(3)根据上述数据,计算xMgCO3•yMg(OH)2•zH2O中x:y:z的最简比;
(提示:MgCO3═MgO+CO2↑、Mg(OH)2═MgO+H2O)
(4)根据上述实验结论,结合“固体质量-温度关系图”(如图2),回答下列问题:
①当温度达360℃时,固体质量减少了3.6g,此质量是生成的水的质量;
②反应完全进行时,温度最低为360℃,此时热分解装置中的剩余固体物质为碳酸镁和氢氧化镁.
12.做下列物质在氧气中燃烧的实验之前,不必在集气瓶底放水或铺沙的是( )
| A. | 木炭在氧气中燃烧 | B. | 铁丝在氧气中燃烧 | ||
| C. | 硫在氧气中燃烧 | D. | 红磷在氧气中燃烧 |