题目内容
2.用R表示某化合物的化学式,R在一定条件下有如下反应:R+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O.下列说法不正确的是( )| A. | R由碳、氢、氧三种元素组成 | B. | R中碳元素的质量分数约为52.2% | ||
| C. | R的相对分子质量是46 | D. | R中碳、氢两种元素的质量比为1:3 |
分析 根据化学方程式可以判断物质的化学式,根据物质的化学式可以判断物质的元素组成、相对分子质量、组成元素的质量分数及其质量比.
解答 解:由R+3O2 $\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O可知,反应前:C:0,H:0,O:6;反应后:C:2,H:6,O:7,故R是C2H6O.
A、R由碳、氢、氧三种元素组成.正确;
B、R中碳的质量分数为:$\frac{24}{46}$×100%=52.3%.正确;
C、R的相对分子质量为:12×2+1×6+16=46.正确;
D、R中碳、氢两种元素的质量比为:(12×2):(1×6)=4:1,故错误.
故选D.
点评 在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变.

练习册系列答案
相关题目
8.水和溶液在生命活动和生活中起着十分重要的作用.
(1)海水中含有大量的氯化钠,可以通过日晒方法获得粗盐,粗盐提纯得到精盐.
(2)0.9%的氯化钠溶液称作生理盐水,其溶质是氯化钠.若用10%的NaCl溶液来配制
100g 0.9%的氯化钠溶液,需加水91g.
(3)熟石灰在部分温度下的溶解度如下表所示.
①20℃时,0.74g熟石灰放入到盛有100g水的烧杯中,搅拌,所得溶液中氢氧化钙的质量0.16,溶液中溶质的质量分数是$\frac{0.16g}{100g+0.16g}$×100%;(写计算式).
②采用一种操作方法,将上述烧杯中剩余固体全部溶解,变为不饱和溶液.下列说法正确的是BC.
A.溶液的质量可能不变 B.溶液中溶质的质量分数一定减小
C.溶液中溶质的质量一定增大 D.可以升温使之变成不饱和溶液.
(1)海水中含有大量的氯化钠,可以通过日晒方法获得粗盐,粗盐提纯得到精盐.
(2)0.9%的氯化钠溶液称作生理盐水,其溶质是氯化钠.若用10%的NaCl溶液来配制
100g 0.9%的氯化钠溶液,需加水91g.
(3)熟石灰在部分温度下的溶解度如下表所示.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 0.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 |
②采用一种操作方法,将上述烧杯中剩余固体全部溶解,变为不饱和溶液.下列说法正确的是BC.
A.溶液的质量可能不变 B.溶液中溶质的质量分数一定减小
C.溶液中溶质的质量一定增大 D.可以升温使之变成不饱和溶液.
13.元素的化学性质由( )决定的.
| A. | 核电荷数 | B. | 中子数 | C. | 电子数 | D. | 最外层电子数 |
17.某溶液中先滴加稀盐酸,无现象,再滴加氯化钡溶液,有白色沉淀产生,该溶液( )
| A. | 一定含有SO42- | B. | 一定含有Ag+ | ||
| C. | 一定含有CO32- | D. | 一定含有Ag+或SO42- |
11.正确的实验操作对实验结果、人身安全非常重要,下列实验操作正确的是( )
| A. |  加热固体 | B. |  取用固体粉末 取用固体粉末 | C. |  倾倒液体 | D. |  点燃酒精灯 |
12.为了经济的可持续发展,我们必须保护水资源,下列做法中,正确的是( )
| A. | 洗蔬菜的水用于浇花 | |
| B. | 为了节约用水,农业和园林的浇灌改为喷灌和滴灌 | |
| C. | 洗水果时要不间断地放水冲洗 | |
| D. | 工业废水处理达标后再排放 |
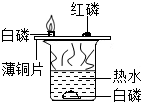 小王用如图所示的装置探究可燃物燃烧的条件.他发现热水中白磷熔化成一白色小液滴.不久,铜片上的白磷开始燃烧,而红磷及水中的白磷不燃烧.请回答:
小王用如图所示的装置探究可燃物燃烧的条件.他发现热水中白磷熔化成一白色小液滴.不久,铜片上的白磷开始燃烧,而红磷及水中的白磷不燃烧.请回答: