题目内容
14.如图是实验室常见的制取气体的装置: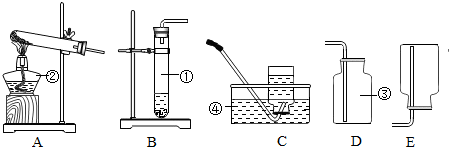
(1)写出仪器名称:①试管②酒精灯③集气瓶④水槽
(2)实验室采用高锰酸钾制取氧气时,试管口还要放一团棉花,目的是防止加热时高锰酸钾粉末进入导管.该反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)采用装置B制取氧气时,其试管中应放的药品是过氧化氢、二氧化锰,该反应的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)收集氧气可以选择装置C或D,原因是氧气不易溶于水、氧气密度比空气大.
分析 (1)据常用仪器回答;
(2)据高锰酸钾制取氧气的注意事项和反应原理解答;
(3)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(4)氧气密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集.
解答 解:(1)标号仪器分别是试管、酒精灯、集气瓶、水槽;
(2)加热高锰酸钾时试管口要放一团棉花,是为了防止加热时高锰酸钾粉末进入导管,加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)采用装置B制取氧气时,说明是在常温下用过氧化氢溶液和二氧化锰制取氧气,二氧化锰在此反应中起催化作用,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)氧气密度比空气大且不易溶于水,所以可用向上排空气法或排水法收集;
故答案为:(1)试管;酒精灯;集气瓶;水槽;
(2)防止加热时高锰酸钾粉末进入导管;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)过氧化氢、二氧化锰;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(4)C;D;氧气不易溶于水;氧气密度比空气大.
点评 本题综合考查了仪器的用途、化学方程式的书写、装置选择、实验基本操作等知识,只有综合理解化学知识才能够正确的解答.

练习册系列答案
相关题目
4.下列实验操作能达到目的是( )
| A. | 向滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,则证明BaCl2有酸性 | |
| B. | 准确称取1.5gCa(OH)2,配制50g 3%的Ca(OH)2溶液 | |
| C. | 在实验室,可无需查阅资料用98%的浓硫酸来配制50g9.8%的稀硫酸溶液 | |
| D. | 可通过灼热的镁粉除去CO2中的O2 |
9.溶液所具有的特征是( )
| A. | 透明的 | B. | 无色的 | C. | 均一稳定的 | D. | 纯净的 |
19.下列装置能达到对应实验目的是( )
| A. |  比较 MnO2和 Fe2O3的催化效果 | B. | 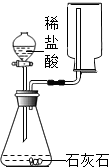 制取并收集CO2气体 | ||
| C. | 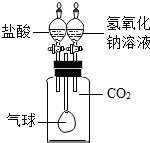 证明 CO2和 NaOH已发生反应 | D. |  形成蓝色喷泉 |
6.下列有关金属的说法错误的是( )
| A. | 合金材料中一定不含非金属 | |
| B. | 人类可以从铁矿石中提取出金属铁 | |
| C. | 生铁的硬度比纯铁的大 | |
| D. | 焊锡是锡铅合金,其熔点远低于纯锡、铅的熔点 |
3.将氢氧化铜沉淀从溶液中分离出来不需用到的仪器是( )
| A. | 烧杯 | B. | 普通漏斗 | C. | 玻璃棒 | D. | 酒精灯 |
 构建化学知识网络是一种重要的学习方法.如图所示是关于铁的化学性质的知识网络(“→”表示一种物质转化另一种物质),其中B是密度最小的气体,C为红色固体单质.请回答下列问题:
构建化学知识网络是一种重要的学习方法.如图所示是关于铁的化学性质的知识网络(“→”表示一种物质转化另一种物质),其中B是密度最小的气体,C为红色固体单质.请回答下列问题: