题目内容
20. 化学物质之间的反应关系也可以构建出一些图形.将铝丝(经砂纸打磨)、稀盐酸、氢氧化钠溶液、氯化铜溶液这四种物质填在合适的位置上,其中C所表示的物质不是单质.(“-”连接的物质能反应,“→”连接的物质能转化)
化学物质之间的反应关系也可以构建出一些图形.将铝丝(经砂纸打磨)、稀盐酸、氢氧化钠溶液、氯化铜溶液这四种物质填在合适的位置上,其中C所表示的物质不是单质.(“-”连接的物质能反应,“→”连接的物质能转化)(1)在图中相应的圆中标出四种物质的化学式;
(2)A与D发生反应的实验现象铝丝表面有红色物质生成,溶液由蓝色变成无色;
(3)请写出有沉淀生成的复分解反应的化学方程式CuCl2+2NaOH=Cu(OH)2↓+2NaCl.
分析 根据B会转化成D,所以B是盐酸,D是氯化铜,C会与盐酸、氯化铜反应,C所表示的物质不是单质,所以C是氢氧化钠,A就是铝丝,然后将推出的物质进行验证即可.
解答 解:(1)B会转化成D,所以B是盐酸,D是氯化铜,C会与盐酸、氯化铜反应,C所表示的物质不是单质,所以C是氢氧化钠,A就是铝丝,经过验证,推导正确,所以A是铝丝,B是盐酸,C是氢氧化钠,D是氯化铜,所以
(2)A与D发生的反应是铝和氯化铜反应生成氯化铝和铜,实验现象为:铝丝表面有红色物质生成,溶液由蓝色变成无色;
(3)有沉淀生成的复分解反应是氢氧化钠和氯化铜反应生成氯化钠和氢氧化铜沉淀,化学方程式为:CuCl2+2NaOH=Cu(OH)2↓+2NaCl.
故答案为:(1)
(2)铝丝表面有红色物质生成,溶液由蓝色变成无色;
(3)CuCl2+2NaOH=Cu(OH)2↓+2NaCl.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
11.化学与食品、药品安全
近年来,食品安全已受到了国人的普遍关注.但是一些不法商贩仍然不顾国家法律,置若罔闻,从瘦肉精到染色馒头、毒豆芽、地沟油、药品胶囊,危害食品安全的事件时有发生.请阅读下列信息,回答有关问题:
事件一:2011年4月11日晚,央视曝光“上海华联超市等销售染色馒头”,商家为了降低成本将柠檬黄用在玉米馒头中着色,山梨酸钾用在馒头中防止馒头发霉,甜蜜素用在馒头中代替蔗糖.面对记者的采访,而染色馒头的生产者对自己生产的馒头却说“我不会吃的,打死我都不会吃,饿死我都不会吃”.
事件二:2011年4月17日,沈阳警方端掉一黑豆芽加工点,老板称这种豆芽“旺季每天可售出2000斤”. 经检验这些“毒豆芽”中含有过量的亚硝酸钠、尿素等有害物质,其中尿素超标27倍,长期食用这种豆芽可致癌.
事件三:2012年4月16日国家食品药品监督管理局发出紧急通知,要求对修正药业等9个厂家,13个药用空心胶囊产品暂停销售和使用.经检验这些用工业明胶制成的胶囊中重金属铬含量超过国家标准规定2mg/kg的限量值,其中超标最多的达90多倍.
(1)馒头是我们的主食之一.食用馒头摄入体内的主要营养物质属于糖类,馒头中的主要成分是淀粉,它在人体内不能直接被吸收,而是在淀粉酶和水的作用下,转变成葡萄糖并溶解在血液中,生成的葡萄糖在体内经缓慢氧化放出热量供肌体活动,这一过程的化学反应方程式为C6H12O6+6O2═6CO2+6H2O.
(2)防腐剂山梨酸钾的化学式为C6H7KO2,试回答:
①山梨酸钾中C、H、K、O各元素的质量比为72:7:39:32;
②山梨酸钾中钾元素的质量分数为26.0%(结果保留1位小数).
(3)亚硝酸钠(NaNO2)是一种白色固体,有咸味,外观与氯化钠相似,有毒,过量或长期食用会对人体产生危害.有关氯化钠和亚硝酸钠的部分资料如表:
①根据上表提供的信息,写出亚硝酸钠的两条化学性质:溶液呈弱碱性、不稳定受热易分解.
②测定亚硝酸钠水溶液的pH约为C(填序号).
A.4 B.6.4 C.7.5 D.13
③工业用盐中常混有亚硝酸钠.为检验某食盐中是否含有亚硝酸钠,你的操作方法是取少量食盐于试管中,然后加热,若有刺激性气味的气体产生,就证明食盐中含有亚硝酸钠..
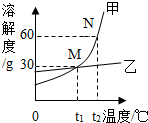
(4)如图3为氯化钠和亚硝酸钠的溶解度曲线,试回答:
①在20℃时,氯化钠饱和溶液中溶质的质量分数小于(填“大于”、“等于”、“小于”)亚硝酸钠的饱和溶液中溶质的质量分数.
②在20℃时,各取氯化钠和亚硝酸钠50g,分别加入到100g水中充分搅拌后,得到的亚硝酸钠溶液属于不饱和(填“饱和”或“不饱和”)溶液.
(5)食用铬含量超标的药品胶囊,会使人中毒的原因是铬是重金属,人体中具有生命活性的物质是蛋白质,当人体摄入重金属铬盐后,蛋白质的结构就会被破坏,生理活性随之消失.
近年来,食品安全已受到了国人的普遍关注.但是一些不法商贩仍然不顾国家法律,置若罔闻,从瘦肉精到染色馒头、毒豆芽、地沟油、药品胶囊,危害食品安全的事件时有发生.请阅读下列信息,回答有关问题:

事件一:2011年4月11日晚,央视曝光“上海华联超市等销售染色馒头”,商家为了降低成本将柠檬黄用在玉米馒头中着色,山梨酸钾用在馒头中防止馒头发霉,甜蜜素用在馒头中代替蔗糖.面对记者的采访,而染色馒头的生产者对自己生产的馒头却说“我不会吃的,打死我都不会吃,饿死我都不会吃”.
事件二:2011年4月17日,沈阳警方端掉一黑豆芽加工点,老板称这种豆芽“旺季每天可售出2000斤”. 经检验这些“毒豆芽”中含有过量的亚硝酸钠、尿素等有害物质,其中尿素超标27倍,长期食用这种豆芽可致癌.
事件三:2012年4月16日国家食品药品监督管理局发出紧急通知,要求对修正药业等9个厂家,13个药用空心胶囊产品暂停销售和使用.经检验这些用工业明胶制成的胶囊中重金属铬含量超过国家标准规定2mg/kg的限量值,其中超标最多的达90多倍.
(1)馒头是我们的主食之一.食用馒头摄入体内的主要营养物质属于糖类,馒头中的主要成分是淀粉,它在人体内不能直接被吸收,而是在淀粉酶和水的作用下,转变成葡萄糖并溶解在血液中,生成的葡萄糖在体内经缓慢氧化放出热量供肌体活动,这一过程的化学反应方程式为C6H12O6+6O2═6CO2+6H2O.
(2)防腐剂山梨酸钾的化学式为C6H7KO2,试回答:
①山梨酸钾中C、H、K、O各元素的质量比为72:7:39:32;
②山梨酸钾中钾元素的质量分数为26.0%(结果保留1位小数).
(3)亚硝酸钠(NaNO2)是一种白色固体,有咸味,外观与氯化钠相似,有毒,过量或长期食用会对人体产生危害.有关氯化钠和亚硝酸钠的部分资料如表:
| 物质名称 | 水溶性 | 熔点 | 溶液的酸碱性 | 热稳定性 | 与稀盐酸作用 |
| 亚硝酸钠 | 易溶,在15℃时 溶解度为81.5g | 271℃ | 弱碱性 | 320℃以上会分解 放出刺激性气体 | 放出红棕色气体 |
| 氯化钠 | 易溶,在15℃时 溶解度为35.8g | 801℃ | 中性 | 受热不分解 | 不反应 |
②测定亚硝酸钠水溶液的pH约为C(填序号).
A.4 B.6.4 C.7.5 D.13
③工业用盐中常混有亚硝酸钠.为检验某食盐中是否含有亚硝酸钠,你的操作方法是取少量食盐于试管中,然后加热,若有刺激性气味的气体产生,就证明食盐中含有亚硝酸钠..
(4)如图3为氯化钠和亚硝酸钠的溶解度曲线,试回答:
①在20℃时,氯化钠饱和溶液中溶质的质量分数小于(填“大于”、“等于”、“小于”)亚硝酸钠的饱和溶液中溶质的质量分数.
②在20℃时,各取氯化钠和亚硝酸钠50g,分别加入到100g水中充分搅拌后,得到的亚硝酸钠溶液属于不饱和(填“饱和”或“不饱和”)溶液.
(5)食用铬含量超标的药品胶囊,会使人中毒的原因是铬是重金属,人体中具有生命活性的物质是蛋白质,当人体摄入重金属铬盐后,蛋白质的结构就会被破坏,生理活性随之消失.

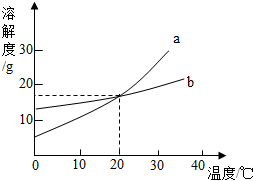
15. 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
 甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )
甲、乙两种不含结晶水的固体物质的溶解度曲线如图,下列说法中正确的是( )| A. | t2℃时,向50g水中加入30g乙可得到80g乙的饱和溶液 | |
| B. | 在t1℃时,两种物质的饱和溶液中溶质的质量相等 | |
| C. | 当甲中混有少量乙时,通常可采用蒸发结晶的方法提纯甲 | |
| D. | t2℃时等质量的两种物质的饱和溶液,降温到t1℃时所得甲、乙饱和溶液的质量一定不相等 |
12.下列实验操作中,正确的是( )
| A. | 配制稀硫酸时,可先在量筒中加入一定量的浓硫酸,再慢慢注入水并不断搅拌 | |
| B. | 蒸发实验中,当蒸发皿内的液体完全蒸干后,立即停止加热 | |
| C. | 用漏斗过滤液体时,液面稍高于滤纸边缘 | |
| D. | 检查装置气密性时,应先把导管一端放入水中,再双手紧捂试管 |
9.甲和乙在一定条件下反应生成丙.结合微观示意图分析,下列结论正确的是( )


| A. | 反应前后分子的总数不变 | B. | 参加反应的甲和乙的质量比为16:1 | ||
| C. | 反应前后原子的种类发生改变 | D. | 反应前后分子的种类发生改变 |
 如图是a、b两种固体物质的溶解度曲线.
如图是a、b两种固体物质的溶解度曲线.


