题目内容
14.利用如图所示实验装置制备常见气体,请回答有关问题: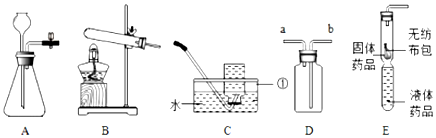
(1)写出标有序号仪器的名称:①水槽.
(2)实验室用高锰酸钾为药品制取氧气,应选择的发生装置是B(填写字母);若用装置C收集的氧气不纯,原因可能是收集氧气前集气瓶中未装满水(写一种);用装置D收集氧气,验满时将带火星的木条放在a(选填“a”或“b”)处.
(3)装置E是用软塑料管自制的气体发生装置,利用该装置可支取二氧化碳气体,软塑料管中液体药品的名称是稀盐酸,药品加入完毕后,接下来的操作是用水攥紧塑料管的下端,使液体与固体接触.
分析 (1)熟记仪器的名称;
(2)根据反应物的状态与反应条件确定制取装置,根据收集氧气的注意事项以及验满的方法来分析;
(3)根据实验室制取二氧化碳的药品以及实验装置的特点来分析.
解答 解:(1)仪器①是水槽;故填:水槽;
(2)用高锰酸钾为药品制取氧气,属于固体加热制取氧气,选择装置B;用排水法收集氧气时,集气瓶内事先应灌满水,否则导致收集的氧气不纯,氧气的密度比空气大,所以用装置D来收集氧气时,氧气从长管进入,所以验满是带火星的木条放在a处;故填:B;收集氧气前集气瓶中未装满水;a;
(3)在实验室中,通常用大理石或石灰石与稀盐酸反应来制取二氧化碳,加入药品后用手攥紧软塑料管的下端,液体与固体混合产生二氧化碳,反之则反应停止.故填:稀盐酸;用水攥紧塑料管的下端,使液体与固体接触.
点评 本题考查了常见气体发生装置和收集装置的选择,完成此题,可以依据已有的知识进行.要求同学们在完成此类题目时,要熟知反应物的状态和反应的条件以及气体的密度和水溶性,以便做出正确的判断.

练习册系列答案
相关题目
17. 在化学反应A2+BC=B+A2C中,反应物BC与生成B的质量关系如图所示.若2g A2与80g BC恰好完全反应,则生成A2C的质量是( )
在化学反应A2+BC=B+A2C中,反应物BC与生成B的质量关系如图所示.若2g A2与80g BC恰好完全反应,则生成A2C的质量是( )
 在化学反应A2+BC=B+A2C中,反应物BC与生成B的质量关系如图所示.若2g A2与80g BC恰好完全反应,则生成A2C的质量是( )
在化学反应A2+BC=B+A2C中,反应物BC与生成B的质量关系如图所示.若2g A2与80g BC恰好完全反应,则生成A2C的质量是( )| A. | 8g | B. | 18g | C. | 28 g | D. | 80g |
2.甲组同学往20克10%的氢氧化钠溶液样品中滴加10% 的盐酸(室温下).如图描述的是氢氧化钠与盐酸反应的微观实质.
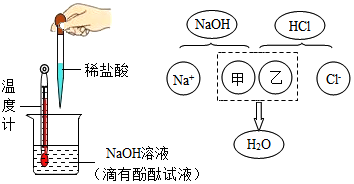
(1)从分类角度:氢氧化钠属于C.
A、氧化物 B、酸 C、碱 D、盐
(2)从宏观与微观角度:
?请从微观的角度分析,甲、乙处应填入的化学符号依次是OH-、H+.
请用离子符号表示酸碱中和反应的本质:OH-+H+=H2O.
?判断在盐酸溶液中一定能大量共存的离子组是D
A、Na+、K+、CO32- B、Ag+、NO3-、SO42-
C、Cu2+、NO3-、OH- D、K+、NH4+、SO42-
(3)从能量角度
反应中溶液温度的变化 记录如表,据表数据分析:
①当加入盐酸体积为6mL时,表明NaOH与HCl恰好完全反应.此判断的依据是此时温度上升最高.
②当加入4mL盐酸时,烧杯中溶液仍然呈红色,该溶液中含有的溶质有酚酞和NaCl、NaOH.(写化学式)

(1)从分类角度:氢氧化钠属于C.
A、氧化物 B、酸 C、碱 D、盐
(2)从宏观与微观角度:
?请从微观的角度分析,甲、乙处应填入的化学符号依次是OH-、H+.
请用离子符号表示酸碱中和反应的本质:OH-+H+=H2O.
?判断在盐酸溶液中一定能大量共存的离子组是D
A、Na+、K+、CO32- B、Ag+、NO3-、SO42-
C、Cu2+、NO3-、OH- D、K+、NH4+、SO42-
| 加入盐酸的体积(V)/mL | 2 | 4 | 6 | 8 | 10 |
| 溶液温度上升(△t)/℃ | 5.6 | 12.1 | 18.5 | 15.2 | 13.5 |
反应中溶液温度的变化 记录如表,据表数据分析:
①当加入盐酸体积为6mL时,表明NaOH与HCl恰好完全反应.此判断的依据是此时温度上升最高.
②当加入4mL盐酸时,烧杯中溶液仍然呈红色,该溶液中含有的溶质有酚酞和NaCl、NaOH.(写化学式)
9.下列溶液中,pH大于7的是( )
| A. | 稀氢氧化钠溶液 | B. | 稀盐酸 | C. | 氯化钠溶液 | D. | 稀硫酸 |
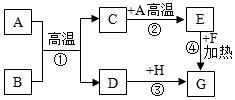 A~H是初中化学常见的物质,已知A为黑色固体单质,G为紫红色固体单质,B为红棕色粉末,H为蓝色的硫酸盐溶液.它们的转化关系如图所示,回答问题:
A~H是初中化学常见的物质,已知A为黑色固体单质,G为紫红色固体单质,B为红棕色粉末,H为蓝色的硫酸盐溶液.它们的转化关系如图所示,回答问题:
 根据下列装置回答问题.
根据下列装置回答问题. 不同年龄段的群体每天钙的适宜摄入量不同,如图为某保健品说明书的一部分,请回答:
不同年龄段的群体每天钙的适宜摄入量不同,如图为某保健品说明书的一部分,请回答: