题目内容
7.下列各组物质在给定条件下能大量共存的是( )| A. | 在 pH=1的溶液中:NaCl、Na2CO3、Na2SO4 | |
| B. | 在 pH=2的溶液中:BaCl2、NaNO3、NaOH | |
| C. | 在 pH=3的溶液中:KCl、Na2SO4、HNO3 | |
| D. | 在 pH=14的溶液中:FeCl3、Ba(NO3)2、CaCl2 |
分析 pH=1、2、3的溶液显酸性,水溶液中含有大量的H+;pH=14的溶液显碱性,水溶液中含有大量的OH-.根据复分解反应的条件,离子间若能互相结合成沉淀、气体或水,则离子不能大量共存,据此进行分析判断即可.
解答 解:A、pH=1的溶液显酸性,水溶液中含有大量的H+;Na2CO3与酸性溶液中的H+两种离子能结合成水和二氧化碳,不能大量共存,故选项错误.
B、pH=2的溶液显酸性,水溶液中含有大量的H+;NaOH与酸性溶液中的H+两种离子能结合成水,不能大量共存,故选项错误.
C、pH=3的溶液显酸性,水溶液中含有大量的H+;离子间不能结合成沉淀、气体或水,能大量共存,故选项正确.
D、pH=14的溶液显碱性,水溶液中含有大量的OH-;FeCl3与碱性溶液中的OH-结合生成氢氧化铁红褐色沉淀,故选项错误.
故选:C.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水.

练习册系列答案
相关题目
12.由Zn、CuO、稀H2SO4作原料,通过两种途径制取Cu:
(1)CuO+H2SO4=CuSO4+H2O Zn+CuSO4=ZnSO4+Cu
(2)Zn+H2SO4=ZnSO4+H2 CuO+H2═Cu+H2O
要制得相同质量的铜(假设每一步反应都很完全),对于两种途径,现有如下说法:
①消耗相同质量的硫酸 ②消耗相同质量的Zn
③消耗相同质量的CuO ④生成相同质量的ZnSO4
下列结论正确的是( )
(1)CuO+H2SO4=CuSO4+H2O Zn+CuSO4=ZnSO4+Cu
(2)Zn+H2SO4=ZnSO4+H2 CuO+H2═Cu+H2O
要制得相同质量的铜(假设每一步反应都很完全),对于两种途径,现有如下说法:
①消耗相同质量的硫酸 ②消耗相同质量的Zn
③消耗相同质量的CuO ④生成相同质量的ZnSO4
下列结论正确的是( )
| A. | 都正确 | B. | 都不正确 | C. | 仅①②③正确 | D. | 仅③正确 |
19.下列物质在pH=1的溶液中能够大量共存,且形成无色溶液的是( )
| A. | CaCl2、NaOH、KNO3、Mg(NO3)2 | B. | FeCl3、H2SO4、KCl、NaNO3 | ||
| C. | NaHCO3、KCl、NH4NO3、Na2SO4 | D. | Mg(NO3)2、Na2SO4、NH4Cl、KNO3 |
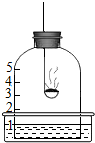 如图装置所示,将钟罩放入盛水的水槽中,以水面为基准线,将钟罩水面以上容积分为5等份.在燃烧匙内盛过量红磷,用酒精灯点燃后,立即插入钟罩内,塞紧橡皮塞.请问:
如图装置所示,将钟罩放入盛水的水槽中,以水面为基准线,将钟罩水面以上容积分为5等份.在燃烧匙内盛过量红磷,用酒精灯点燃后,立即插入钟罩内,塞紧橡皮塞.请问: