题目内容
2.某校化学兴趣小组的同学利用下列装置进行实验.实验目的:
(1)用高锰酸钾制取一瓶氧气,做细铁丝燃烧的实验.
(2)粗略测定加热2克高锰酸钾所收集到的氧气体积.
(用化学方程式表示)细铁丝在氧气中燃烧:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4
仪器认识:写出仪器①②的名称:①试管②量筒
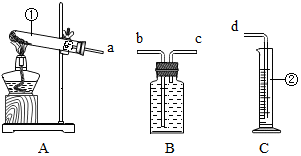
装置连接:为达到实验目的(2),各装置的正确连接顺序是:(填接口的字母)
a→c→b→d
问题分析:(1)实验过程中发现B瓶中的水变红了,原因是:试管口没放棉花,高锰酸钾随气流进入导气管
(2)用收集到的氧气做细铁丝试验时,发现瓶底炸裂,发生失误的操作原因可能是:集气瓶底部未放水或一些沙子
(3)请根据化学方程式计算出理论上2克高锰酸钾完全分解可生成多少克氧气?
(4)同学们在实际中测得氧气在标准状况下的体积为177毫升,换算成质量为0.253克,超过理论量.从理论上推测:你认为超过理论量的氧气可能来源于什么物质?K2MnO4、MnO2(写出所有可能,空气、水因素忽略不计).
分析 反应原理:①高锰酸钾制氧气:知其反应物为高锰酸钾,生成物为锰酸钾、二氧化锰、氧气,反应条件为加热,可书写化学方程式;②细铁丝在氧气中燃烧:知其反应物为铁和氧气,生成物为四氧化三铁,反应条件为点燃,可书写出化学方程式;
仪器认识:了解常用仪器的名称和应用,即可轻松解答;
装置连接:为达到实验目的粗略测定加热2g高锰酸钾所收集到的氧气体积,则各装置的正确连接顺序是a→c→b→d;
问题分析:由图知:(1)装置A试管口缺少一团棉花,会导致KMnO4进入导管,进入B瓶,使水变红;
(2)铁丝燃烧实验集气瓶应保留少量水,以免细铁丝在氧气中燃烧,瓶底炸裂;
(3)根据化学方程式的计算依据反应物可求生成物;
(4)中水的体积即为收集的氧气的体积.制得氧气的实际量高于理论量,题中提示除去可能混有空气、水因素外,只可能来源于含有氧元素的生成物K2MnO4、MnO2.
解答 解:反应原理:高锰酸钾加热生成锰酸钾、二氧化锰和氧气,反应方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;铁丝与氧气在点燃的条件下生成四氧化三铁,方程式是:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;
仪器认识:标号仪器分别是试管和量筒;
装置连接:要测定分解高锰酸钾所得到的氧气的体积,由于氧气不易溶于水,所以可将气体通过B装置,利用排水法收集氧气,排出的水的体积即是生成的氧气的体积;通入氧气应从c进入,随着瓶内气压增大,将水从b压入量筒内,从而测量出生成氧气的体积;
故答案为:c→b;
问题分析:
(1)实验过程中发现B瓶中的水变红了,原因是:试管口没放棉花,高锰酸钾随气流进入导气管;
(2)用收集到的氧气做细铁丝燃烧的实验时,发现瓶底炸裂,发生失误的操作原因可能是:瓶底未放水或一些沙子;
(3)设加热2g高锰酸钾完全分解,可生成氧气的质量为x
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
2×158 32
2g x
$\frac{2×158}{2g}=\frac{32}{x}$
x=0.2025g
(4)C中水的体积即为收集的氧气的体积,制得氧气的实际量高于理论量,超出的氧气不会凭空产生,因为题中提示除去可能混有空气、水因素外,依据质量守恒定律化学反应前后元素的种类不变,只可能来源于含有氧元素的是K2MnO4、MnO2.
故答案为:
实验目的:
(2)3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;试管;量筒;c→b;
问题分析:
(1)试管口没放棉花,高锰酸钾随气流进入导气管;
(2)集气瓶底部未放水或一些沙子;
(3)理论上2克高锰酸钾完全分解可生成氧气的质量为0.2025g;
(4)K2MnO4、MnO2
点评 掌握实验室用高锰酸钾制取氧气的反应原理,测量气体体积的方法,铁丝燃烧的相关知识即可正确该题.

 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案| A. | 铝箔在氧气中燃烧,发出耀眼的光 | |
| B. | 硫在氧气中燃烧,发出明亮的蓝紫色火焰 | |
| C. | 铁丝在氧气中燃烧,火星四射,生成黑色固体物质 | |
| D. | 木炭在氧气中燃烧,发出明亮的白光,并形成白雾 |
| A. |  木炭 | B. |  红磷 | C. |  铁丝 | D. |  硫粉 |
| A. | 紫色→红色→红色 | B. | 紫色→蓝色→无色 | C. | 紫色→红色→紫色 | D. | 紫色→红色→无色 |
| A. | 在 pH=1的溶液中:NaCl、Na2CO3、Na2SO4 | |
| B. | 在 pH=2的溶液中:BaCl2、NaNO3、NaOH | |
| C. | 在 pH=3的溶液中:KCl、Na2SO4、HNO3 | |
| D. | 在 pH=14的溶液中:FeCl3、Ba(NO3)2、CaCl2 |
| A. | 蒸发掉1克水,有少量固体析出 | |
| B. | 降低温度,有少量固体析出 | |
| C. | 烧杯底部还有少量未溶的硝酸钾固体 | |
| D. | 加入少量水,没有固体析出 |