题目内容
11.节假日或双休日,去郊游野炊实为一大快事.然而,在野炊的情趣之中,如果遇到下面一些问题,你是如何处理的?(1)对野炊有经验的人会告诉你,餐具最好是导热性好,不易破碎的材料制的,你准备带的餐具是用A(填字母)制的.
A.金属 B.陶瓷 C.无所谓
(2)在“灶”上悬挂野炊锅时,应调节野炊锅到合适的高度.你觉得原因可能是便于使用外焰加热;
(3)野餐食谱如下:主食:馒头 配菜:烤火腿、鲫鱼汤、五香豆干,从营养角度来看,你准备再添一样C(填字母).
.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(4)在引燃细枯枝后,如果迅速往“灶”里塞满枯枝,结果反而燃烧不旺,并产生很多浓烟,说明物质充分燃烧需要的条件是使可燃物与空气(或氧气)充分接触;
(5)若不小心被蚊虫叮咬(蚊虫能分泌出蚁酸),下列物质可用于涂抹以减轻疼痛的是C(填字母).
A.食醋(pH<7)B.食盐水(pH=7)C.肥皂水(pH>7)
(6)郊外通常比较泥泞,如果你的交通工具是自行车,你回来进行清洗后是如何防锈的AB.(填字母)
A.立即晾晒干 B.链条传动部件涂上油 C.涂油漆.
分析 (1)根据餐具具备的特点进行分析解答,从导热性好,不易破碎方面考虑选择材料;
(2)根据燃烧的条件进行分析解答;
(3)根据食物所含的营养素进行分析解答,所给食品中缺少维生素;
(4)根据促进燃烧的方法进行解答;
(5)根据酸碱中和反应进行解答;
(6根据防锈的措施进行解答.
解答 解:(1)金属既具有良好的导热性,又具有不易破碎的性质,所以适合野炊餐具用;故答案为:A;
(2)调节野炊锅到合适的高度,可以使可燃物于氧气充分接触;木柴必须要干燥才容易点着,原因是易于达到木柴的着火点,故答案为:便于使用外焰加热;
(3)馒头中含有淀粉即糖类,烤火腿、鲫鱼汤、五香豆干中含有丰富的蛋白质、脂肪、无机盐、水,唯独缺少维生素,水果、蔬菜中含有丰富的维生素;故答案为:C;
(4)物质充分燃烧需要与氧气充分接触,故填:使可燃物与空气(或氧气)充分接触;
(5)蚊虫能分泌出蚁酸,则所用的物质应该是碱性的;A食醋(pH<7),呈酸性,错误;B食盐水(pH=7),呈中性,错误,C肥皂水(pH>7),呈碱性,错误;故填:C
(6)防锈就是破坏铁生锈的条件,A.立即晾晒干可以隔绝水,能防锈; B.链条传动部件涂上油可以隔绝氧气和水,能防锈;C.涂油漆可以防锈,但是不符合实际情况;故填:AB.
点评 野炊餐具最好用金属制的,导热性好并且不易破碎;加热时一般用外焰加热;要均衡膳食;燃烧时要使可燃物燃烧充分.

练习册系列答案
相关题目
1.除去密闭容器里空气中的氧气,得到较纯净的氮气,可采用燃烧除去氧气的方法,下列物质可选用的是( )
| A. | 硫 | B. | 木炭 | C. | 红磷 | D. | 氢气 |
2.下列关于化学反应X2+3Y2═2Z的叙述错误的是( )
| A. | Z的化学式为XY3 | |
| B. | 该方程式可表示1个X2分子与3个Y2分子反应生成了2个Z分子 | |
| C. | 若 X2和Y2的相对分子质量分别是M和N,则Z的相对分子质量为(M+N) | |
| D. | 若agX2完全反应生成 b g Z,则同时消耗(b-a)g Y2 |
16.熟石灰在部分温度下的溶解度如下表所示.
(1)20℃时,0.56g氧化钙放入到盛有100g水的烧杯中.恢复到20℃时,所得溶液中水的质量减小(填“增大”“减小”或“不变”),溶液中溶质的质量分数是$\frac{0.16g}{0.16g+100g}$×100%(写计算式).
(2)采用一种操作方法,将上述烧杯中剩余固体全部溶解,变为不饱和溶液.下列说法正确的是B.
A.溶液的质量可能不变
B.溶液中溶质的质量分数一定减小
C.溶液中溶质的质量一定增大
D.可以升温使之变成不饱和溶液.
| 温度/℃ | O | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | O.18 | 0.17 | 0.16 | 0.15 | 0.14 | 0.13 | 0.12 |
(2)采用一种操作方法,将上述烧杯中剩余固体全部溶解,变为不饱和溶液.下列说法正确的是B.
A.溶液的质量可能不变
B.溶液中溶质的质量分数一定减小
C.溶液中溶质的质量一定增大
D.可以升温使之变成不饱和溶液.
3.化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:
【查得资料】(1)该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生.
(2)饱和碳酸氢钠溶液不吸收二氧化碳.
【设计实验】小组同学设计了如图所示装置(图中夹持仪器略去) 测定牙膏样品中碳酸钙的含量.
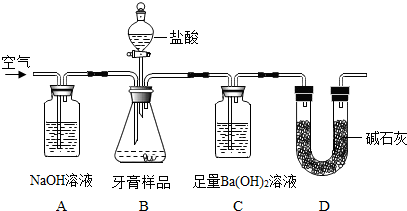
依据图示回答下列问题:
(1)该装置中氢氧化钠溶液的作用是吸收空气中的二氧化碳.
(2)C中观察到有沉淀产生,反应的化学方程式为CO2+Ba(OH)2=BaCO3↓+H2O.
(3)实验过程中需持续缓缓通入空气,其作用有使反应产生的二氧化碳全部被氢氧化钡溶液吸收.
【解释与结论】实验测得如下数据:
欲计算样品中碳酸钙的含量,应选择的数据是三组数据的平均值.
【反思与评价】
(1)有人认为不必测定C中沉淀的质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是氢氧化钡溶液吸收了挥发出的氯化氢气体.
(2)反思实验过程,小刚同学提出应采取必要措施,提高测定准确度.他提出的下列各项措施中,不能提高测定准确度的是bcd(填字母序号).
a.在加入盐酸之前,排净装置内的CO2气体
b.放慢滴加盐酸的速度
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置.
【查得资料】(1)该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生.
(2)饱和碳酸氢钠溶液不吸收二氧化碳.
【设计实验】小组同学设计了如图所示装置(图中夹持仪器略去) 测定牙膏样品中碳酸钙的含量.

依据图示回答下列问题:
(1)该装置中氢氧化钠溶液的作用是吸收空气中的二氧化碳.
(2)C中观察到有沉淀产生,反应的化学方程式为CO2+Ba(OH)2=BaCO3↓+H2O.
(3)实验过程中需持续缓缓通入空气,其作用有使反应产生的二氧化碳全部被氢氧化钡溶液吸收.
【解释与结论】实验测得如下数据:
| 实验次数 | 样品质量(g) | 所用盐酸质量(g) | 所得沉淀质量(g) |
| 第一次 | 8.00 | 50 | 1.95 |
| 第二次 | 8.00 | 50 | 1.98 |
| 第三次 | 8.00 | 50 | 1.96 |
【反思与评价】
(1)有人认为不必测定C中沉淀的质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是氢氧化钡溶液吸收了挥发出的氯化氢气体.
(2)反思实验过程,小刚同学提出应采取必要措施,提高测定准确度.他提出的下列各项措施中,不能提高测定准确度的是bcd(填字母序号).
a.在加入盐酸之前,排净装置内的CO2气体
b.放慢滴加盐酸的速度
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置.

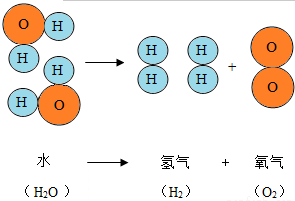 如图是水分子分解示意图,下列说法正确的是( )
如图是水分子分解示意图,下列说法正确的是( )