题目内容
12.在“质量守恒定律”的教学中,老师引导同学们进行“化学反应中反应物与生成物的质量关系”的实验探究,请你参与探究并回答有关问题: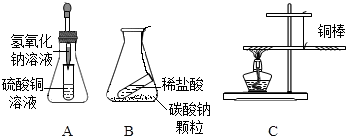
(1)如图A、图B所示,将锥形瓶(反应物未接触)放在天平上,右盘加砝码使之平衡,取下锥形瓶,将锥形瓶中两种物质混合,反应完全后将锥形瓶再放回天平左盘上.
①A瓶试管中发生反应的化学方程式为2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;
把A瓶重新放回到天平上,天平能(选填“能”或“不能”)保持平衡.
②把B瓶重新放回到天平上,天平不能(选填“能”或“不能”)保持平衡,理由是B瓶中所发生的反应中有气体生成,且容器是敞口的,生成的气体逸散到空气中.
③从原子的角度分析化学反应遵守“质量守恒定律”的原因是在化学反应前后原子的种类没有改变,原子的数量没有增减,且原子的质量也没有发生改变.
(2)如图C所示,用细线系住铜棒使之平衡,然后在铜棒一端用酒精灯加热.
①写出铜棒反应的化学方程式:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
②加热一段时间后,铜棒不能(选填“能”或“不能”)保持平衡.
③本实验现象与质量守恒定律没有(选填“有”或“没有”)矛盾.
分析 (1)
①硫酸铜溶液和氢氧化钠混合反应生成氢氧化铜沉淀和硫酸钠,A瓶中的反应没有气体生成也没有气体参与反应,所以反应前后物质的总重量不变,可以据此解答该题;
②B瓶中所发生的反应中有气体生成,且容器是敞口的,所以反应前后B瓶中的质量不再相等,可以据此解答该题;
③根据化学反应的实质来进行解答该题;
(2)铜与氧气反应生成了氧化铜,所以可以判断在加热前后铜棒不能再保持平衡,化学反应遵循质量守恒定律,可以据此解答该题.
解答 解:(1)①硫酸铜溶液和氢氧化钠混合反应生成氢氧化铜沉淀和硫酸钠,反应的化学方程式是2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.
A瓶中的反应没有气体生成也没有气体参与反应,所以反应前后物质的总重量不变,所以A瓶重新放回到天平上,天平能保持平衡;
②B瓶中所发生的反应中有气体生成,且容器是敞口的,所以反应前后B瓶中的质量不再相等,所以B瓶重新放回到天平上,天平不能保持平衡;
③根据化学反应的实质可以知道,在化学反应中原子的种类没有改变,原子的数量没有增减,且原子的质量也没有发生改变,所以在化学反应前后物质的总量不变,即质量守恒;
(2)左端的铜在加热的条件下与氧气反应生成了氧化铜,反应的化学方程式为:2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO.
所以可以判断在加热前后铜棒不能再保持平衡.由于氧气参与反应,所以反应后固体质量增加,本实验现象与质量守恒定律不矛盾.
故答案为:
(1)
①2NaOH+CuSO4=Cu(OH)2↓+Na2SO4;能;
②不能;B瓶中所发生的反应中有气体生成,且容器是敞口的,生成的气体逸散到空气中;
③在化学反应前后原子的种类没有改变,原子的数量没有增减,且原子的质量也没有发生改变;
(2)2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO;不能;没有.
点评 通过回答本题知道了质量守恒定律的微观解释,知道了验证质量守恒定律实验的设计方法,如果有气体放出的反应要在密闭容器中进行.

| A. | 氧气具有可燃性 | |
| B. | 鱼、虾等能在水中生存,是由于氧气易溶于水 | |
| C. | 物质与氧气发生的反应都是氧化反应 | |
| D. | 细铁丝在氧气中剧烈燃烧,生成氧化铁 |
| A. | 均一的、稳定的液体都是溶液 | B. | 溶液都是无色、澄清、透明的 | ||
| C. | 蔗糖、面粉都能在水中形成溶液 | D. | 可用水区分NaOH固体和NH4NO3固体 |
 把盛满甲、乙、丙三种气体的试管分别同时倒插入盛有水的烧杯中并轻轻摇动,一段时间后,观察到如图所示的现象,下列对甲、乙、丙三种气体的分析中正确的是( )
把盛满甲、乙、丙三种气体的试管分别同时倒插入盛有水的烧杯中并轻轻摇动,一段时间后,观察到如图所示的现象,下列对甲、乙、丙三种气体的分析中正确的是( )| A. | 甲、乙、丙气体都易溶于水 | B. | 乙气体比甲气体在水中的溶解度大 | ||
| C. | 不可以用排水集气法收集甲气体 | D. | 可以用向下排空气法收集丙气体 |
| A. | 锈铁钉 | B. | 山泉水 | C. | 液态氧 | D. | 石灰水 |
| A. | 只要发现着火,立即用水浇灭 | |
| B. | 天然气泄漏,立即关闭阀门并开窗通风 | |
| C. | 燃放烟花爆竹时,远离人群和可燃物 | |
| D. | 燃着的酒精灯不慎碰倒,立即用湿布盖灭 |
| A. | Na2SO4、KCl、CuSO4 | B. | KNO3、NaCl、HCl | ||
| C. | H2SO4、FeCl3、NaCl | D. | FeCl2、KCl、NaOH |
| 试 管 | A | B | C | D | E | F |
| CuSO4溶液/毫升 | 0 | 0.5 | 1 | 1.5 | 2 | 4 |
| 水/毫升 | 4 | 3.5 | 3 | 2.5 | 2 | 0 |
| 收集H2所用的时间/秒 | 348 | 246 | 190 | 165 | 230 | 360 |
(2)六组实验中,小明都将水和CuSO4溶液的总体积设定为相同值,目的是控制硫酸铜溶液的总体积相同,只是浓度不同;
(3)由上表可得知,CuSO4溶液的量对稀硫酸与锌反应速率影响是随CuS04溶液的量增加,反应速率先增大后减小.
 如图表示物质间的从属关系,下列选项中符合图形关系是( )
如图表示物质间的从属关系,下列选项中符合图形关系是( )