题目内容
16.请从微观的角度认识物质的构成及化学变化的本质.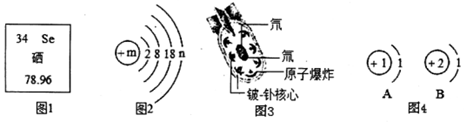
(1)图1、图2表示同一种元素Se,则图2中n=6;硒元素位于元素周期表中的第四周期.
(2)图3是氢弹的结构图,其中钋、铍元素属于金属元素(填“金属”或“非金属”),氘原子核内有一个质子和一个中子,则图4中表示氘原子的是A(填“A”或“B”).
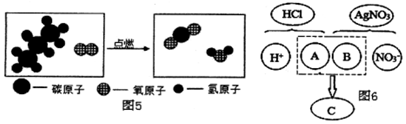
①写出图5中发生的化学方程式C3H8+5O2$\frac{\underline{\;点燃\;}}{\;}$3CO2+4H2O.
②从微观的角度说明图6中反应能够发生的有原因银离子与氯离子能结合成氯化银沉淀.
分析 (1)根据原子中,质子数=核外电子数来分析;根据周期数=原子核外电子层数来分析;
(2)根据元素的分类、原子结构示意图来分析;
(3)①根据微观反应示意图的信息来分析解答;
②根据复分解反应发生的条件来分析.
解答 解:(1)原子中,原子序数=核电荷数=质子数=核外电子数,由元素周期表的信息可知,m=34,则n=34-2-8-18=6;周期数=原子核外电子层数,硒原子的核外有4个电子层,则硒元素位于元素周期表中的第四周期.故填:6;四;
(2)由钋、铍元素的汉语名称偏旁“金”可知,均属于金属元素;氘原子核内有一个质子和一个中子,核外有1个电子,其原子结构示意图为A;故填:金属;A;
(3)①由微观反应示意图可知,该反应是由C3H8与氧气在点燃的条件下反应生成二氧化碳和水,反应的方程式为:C3H8+5O2$\frac{\underline{\;点燃\;}}{\;}$3CO2+4H2O;故填:C3H8+5O2$\frac{\underline{\;点燃\;}}{\;}$3CO2+4H2O;
②盐酸与硝酸银发生复分解反应生成氯化银沉底和硝酸,从微观角度看反应的原因是银离子与氯离子能结合成氯化银沉淀;故填:银离子与氯离子能结合成氯化银沉淀.
点评 本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、原子结构示意图的含义是正确解答本题的关键.

练习册系列答案
相关题目
7.下列实验操作正确的是( )
| A. |  过滤 | B. |  检查装置气密性 | C. |  取用粉末状药品 | D. |  称量氢氧化钠 |
4.下列有关实验描述正确的是( )
| A. | 加热试管中的溶液时,拇指按在试管夹的短柄上 | |
| B. | 用胶头滴管吸取溶液时,在滴管伸入溶液前,要先捏紧胶头 | |
| C. | 稀盐酸中滴入紫色石蕊试液,溶液变红,说明酸遇指示剂变色 | |
| D. | 向一定量KOH和Ba(NO3)2混合溶液中逐滴滴加稀H2SO4,不会立即产生沉淀 |
11.“分类”是学习化学的重要方法.下列说法正确的是( )
| A. | 单质:水银、蒸馏水、铁水 | B. | 有机物:蛋白质、淀粉、酒精 | ||
| C. | 氧化物:二氧化锰、干冰、氯酸钾 | D. | 混合物:煤、石油、甲烷 |
8.下列各组中的离子,能在溶液中大量共存的是( )
| A. | K+ H+ SO42- OH- | B. | Na+ Ca2+ CO32- NO3- | ||
| C. | Na+ Cl- NO3- Ag+ | D. | Na+ Cu2+ Cl- SO42- |
6.某研究小组为了测定石灰石中碳酸钙的质量分数,取石灰石样品15g加入100g稀盐酸溶液,恰好完全反应(杂质不溶于水,也不与酸反应),产生mg二氧化碳气体,则下列说法中不正确的是( )
| A. | 若m的质量为3.3g,石灰石中碳酸钙的质量分数为50% | |
| B. | 反应后溶液中的粒子为Ca2+和Cl- | |
| C. | 若产生m的质量为4.4g,盐酸的质量分数为7.3% | |
| D. | 若产生m的质量为4.4g,则反应所得溶液中溶质的质量分数为10% |
