题目内容
6.某研究小组为了测定石灰石中碳酸钙的质量分数,取石灰石样品15g加入100g稀盐酸溶液,恰好完全反应(杂质不溶于水,也不与酸反应),产生mg二氧化碳气体,则下列说法中不正确的是( )| A. | 若m的质量为3.3g,石灰石中碳酸钙的质量分数为50% | |
| B. | 反应后溶液中的粒子为Ca2+和Cl- | |
| C. | 若产生m的质量为4.4g,盐酸的质量分数为7.3% | |
| D. | 若产生m的质量为4.4g,则反应所得溶液中溶质的质量分数为10% |
分析 根据二氧化碳和对应的化学方程式求算碳酸钙和HCl的质量,进而求算对应的质量分数
解答 解:
若m的质量为3.3g,设该石灰石样品中碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.3g
$\frac{100}{44}$=$\frac{x}{3.3g}$
x=7.5g
石灰石中碳酸钙的质量分数为50%
若m的质量为4.4g,
设该石灰石样品中碳酸钙的质量为a,稀盐酸中溶质的质量为y,生成氯化钙的质量为z
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 111 44
a y z 4.4g
$\frac{100}{a}$=$\frac{73}{y}$=$\frac{111}{z}$=$\frac{44}{4.4g}$
a=10g
y=7.3g
z=11.1g
盐酸的质量分数为$\frac{7.3g}{100g}$×100%=7.3%
若产生m的质量为4.4g,则反应所得溶液中溶质的质量分数为$\frac{11.1g}{10g+100g-4.4g}$×100%≈10.5%
而无论哪种情况都是生成了氯化钙,存在微粒就是钙离子和氯离子,为Ca2+和Cl-.
故选:D.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
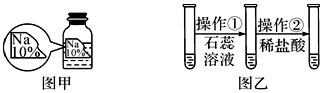
14.某同学在实验室发现了一瓶标签残缺的无色溶液﹙如图甲所示﹚,为确认其中的溶质,他设计并进行了如下探究活动,请回答下列问题.
【猜想与假设】:其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种.
【资料查阅】上述四种物质的相关信息如下:
【探究过程】
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是石蕊试液变成蓝色;在进行操作②时有无色无味的气体产生,由此又可排除假设物质中的氢氧化钠.
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的碳酸钠,你的判断依据是碳酸氢钠饱和溶液的质量分数不可能达到10%,而碳酸钠溶液可以.

【猜想与假设】:其溶质可能为NaCl、NaOH、Na2CO3和NaHCO3中的一种.
【资料查阅】上述四种物质的相关信息如下:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
| 常温下其稀溶液的pH | 7 | 13 | 11 | 9 |
如图乙所示,在操作①后可确定溶质不是NaCl,则其实验现象应是石蕊试液变成蓝色;在进行操作②时有无色无味的气体产生,由此又可排除假设物质中的氢氧化钠.
【探究结论】
你认为该溶液中的溶质可能是上述假设物质中的碳酸钠,你的判断依据是碳酸氢钠饱和溶液的质量分数不可能达到10%,而碳酸钠溶液可以.
1.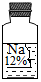 某小组对实验室中一瓶标签受损的无色溶液(如图所示)
某小组对实验室中一瓶标签受损的无色溶液(如图所示)
【提出问题】这瓶无色溶液是什么呢?
【作出猜想】(1)该溶液是NaCl溶液
(2)该溶液是Na2CO3溶液
(3)该溶液是NaHCO3溶液
(4)该溶液是NaOH或NaNO3或Na2SO4溶液(填一种即可).
【查阅资料】常温下的几种物质的溶解度如下表:
【交流讨论】该小组同学讨论后一致认为猜想(3)不正确,理由是常温下碳酸氢钠的饱和溶液的溶质质量分数不可能达到12%.
【实验探究】为确定该溶液成分,同学们进行了如下实验:
【反思评价】
(1)为了防止标签受损,倾倒液体时应注意标签向着手心.
(2)同学们经过讨论后认为实验2得出的结论不正确,原因是若该溶液是硫酸钠,也能产生白色沉淀.若往实验2所得的沉淀中加入一种试剂,就可验证猜想(2)是正确的,该反应的化学方程式为BaCO3+2HCl═BaCl2+H2O+CO2↑.
(3)欲将该溶液稀释为5%的溶液,实验步骤为:计算、量取、混匀.
 某小组对实验室中一瓶标签受损的无色溶液(如图所示)
某小组对实验室中一瓶标签受损的无色溶液(如图所示)【提出问题】这瓶无色溶液是什么呢?
【作出猜想】(1)该溶液是NaCl溶液
(2)该溶液是Na2CO3溶液
(3)该溶液是NaHCO3溶液
(4)该溶液是NaOH或NaNO3或Na2SO4溶液(填一种即可).
【查阅资料】常温下的几种物质的溶解度如下表:
| 物质 | NaCl | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 21.5 | 9.6 |
【实验探究】为确定该溶液成分,同学们进行了如下实验:
| 实验操作 | 实验现象 | 实验结论 | |
| 实验1 | 取少量该溶液于试管中,滴入 几滴酚酞溶液 | 溶液变红 | 猜想(1)不正确 |
| 实验2 | 取少量该溶液于试管中,滴入 BaCl2溶液 | 有白色沉淀产生 | 猜想(2)正确 |
(1)为了防止标签受损,倾倒液体时应注意标签向着手心.
(2)同学们经过讨论后认为实验2得出的结论不正确,原因是若该溶液是硫酸钠,也能产生白色沉淀.若往实验2所得的沉淀中加入一种试剂,就可验证猜想(2)是正确的,该反应的化学方程式为BaCO3+2HCl═BaCl2+H2O+CO2↑.
(3)欲将该溶液稀释为5%的溶液,实验步骤为:计算、量取、混匀.
11.下列四组溶液,仅用组内物质就能鉴别出来且均为无色溶液的是( )
| A. | K2CO3、FeCl3、KOH、ZnSO4 | B. | NaCl、MgCl2、K2SO4、CuSO4 | ||
| C. | NH4HCO3、Ba(OH)2、H2SO4、NaNO3 | D. | K2CO3、Na2SO4、BaCl2、NaOH |
18.如图是元素周期表的一部分,请回答相关问题:
(1)氧元素与硫元素位于同一纵行的原因是原子的最外层电子数相同,它们在化学反应中都易得到(填“得到”或“失去”)电子.
(2)10电子微粒指核外是10个电子的微粒,包括分子、原子、离子等.如氖原子、氧离子、水分子.下列微粒属于10电子微粒的是ACD( 多选题,少选不给分)
A 钠离子 B 硫离子 C 氢氧根离子 D 甲烷分子.
| 第一周期 | 1 H | 2 He | ||||||
| 第二周期 | 3 Li | 4 Be | 5 B | 6 C | 7 N | 8 O | 9 F | 10 Ne |
| 第三周期 | 11Na | 12Mg | 13Al | 14Si | 15P | 16S | 17Cl | 18 Ar |
(2)10电子微粒指核外是10个电子的微粒,包括分子、原子、离子等.如氖原子、氧离子、水分子.下列微粒属于10电子微粒的是ACD( 多选题,少选不给分)
A 钠离子 B 硫离子 C 氢氧根离子 D 甲烷分子.
15.下列课外实验没有科学依据的是( )
| A. | 点燃浸有酒精溶液的手绢可能烧不坏 | |
| B. | 用灼烧的方法区别黄铜和黄金 | |
| C. | 用食品级的小苏打和柠檬酸等自制汽水 | |
| D. | 将鸡蛋放入盐水中变成“软壳蛋” |
16.逻辑推理是化学学习中常用的思维方法.下列推理正确的是( )
| A. | 置换反应生成单质和化合物,生成单质和化合物的反应一定是置换反应 | |
| B. | 单质中只含有一种元素,只含有一种元素的物质一定是单质 | |
| C. | 化合物是不同种元素组成的纯净物,不同种元素组成的纯净物一定是化合物 | |
| D. | 活泼金属能与稀酸反应放出气体,能与稀酸反应放出气体的一定是活泼金属 |