题目内容
在常温时,在室内进行二氧化碳与不同溶质质量分数氢氧化钠溶液反应的实验,装置如图1所示:

试管是1.8×18cm的中型试管(约40mL),观察到NaOH液面上升17mL所用的时间见图2
(1)液面上升最快时,氢氧化钠溶液溶质的质量分数约为 %.
(2)为什么氢氧化钠溶液的溶质质量分数很大时,液面上升的速度反而变慢,主要是因为 ;要使上升速度加快,应采用的实验措施是 .

试管是1.8×18cm的中型试管(约40mL),观察到NaOH液面上升17mL所用的时间见图2
(1)液面上升最快时,氢氧化钠溶液溶质的质量分数约为
(2)为什么氢氧化钠溶液的溶质质量分数很大时,液面上升的速度反而变慢,主要是因为
考点:碱的化学性质,有关溶质质量分数的简单计算
专题:常见的碱 碱的通性
分析:根据题目中的图形,结合题意“二氧化碳与不同溶质质量分数氢氧化钠溶液反应”,可推测答案.
解答:解:根据题目中的图形,结合题意“二氧化碳与不同溶质质量分数氢氧化钠溶液反应”,可推测:
(1)液面上升最快时,氢氧化钠溶液溶质的质量分数约为20%,因为从图中可以看出,用时最少;
(2)氢氧化钠溶液的溶质质量分数很大时,氢氧化钠快速与二氧化碳反应,表面生成碳酸钠膜,阻碍二氧化碳与氢氧化钠的反应,所以液面上升的速度反而变慢,要使上升速度加快,应采用的实验措施是震荡试管,使不能形成碳酸钠晶膜.
故答案为:(1)20.
(2)表面生成碳酸钠膜,阻碍二氧化碳与氢氧化钠的反应;震荡试管,使不能形成碳酸钠晶膜.
(1)液面上升最快时,氢氧化钠溶液溶质的质量分数约为20%,因为从图中可以看出,用时最少;
(2)氢氧化钠溶液的溶质质量分数很大时,氢氧化钠快速与二氧化碳反应,表面生成碳酸钠膜,阻碍二氧化碳与氢氧化钠的反应,所以液面上升的速度反而变慢,要使上升速度加快,应采用的实验措施是震荡试管,使不能形成碳酸钠晶膜.
故答案为:(1)20.
(2)表面生成碳酸钠膜,阻碍二氧化碳与氢氧化钠的反应;震荡试管,使不能形成碳酸钠晶膜.
点评:考虑氢氧化钠溶液与二氧化碳的反应.

练习册系列答案
相关题目
如图图象不能正确反应其对应实验操作的是( )
A、 将锌片插入盛有一定量稀硫酸的烧杯中 |
B、 将等质量的镁和锌分别与足量的盐酸反应 |
C、 向t℃的饱和硝酸钾溶液中加入一定量的硝酸钾晶体 |
D、 向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 |
下列判断正确的是( )
| A、不锈钢属于纯净物 |
| B、C60属于化合物 |
| C、纯碱属于碱 |
| D、干冰属于氧化物 |

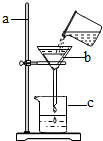 如图是某同学用来除去水中难溶性杂质时所采用的过滤装置图.试回答:
如图是某同学用来除去水中难溶性杂质时所采用的过滤装置图.试回答: