题目内容
19. 某兴趣小组用右图装置(碱石灰是氧化钙和固体氢氧化钠的混合物,极易吸收水蒸汽,经常用作干燥剂),整套装置质量为16克,测定过氧化氢溶液中溶质的质量分数.测得相关数据如下:整套装置16克.
某兴趣小组用右图装置(碱石灰是氧化钙和固体氢氧化钠的混合物,极易吸收水蒸汽,经常用作干燥剂),整套装置质量为16克,测定过氧化氢溶液中溶质的质量分数.测得相关数据如下:整套装置16克.二氧化锰 0.5g称量:整套装置+过氧化氢溶液84.0g称量:整套装置+剩余的混合物83.7g
[称量:整套装置+过氧化氢溶液84.0g]在装置中+[二氧化锰 0.5g]$\stackrel{至质量不再减轻}{→}$[称量:整套装置+剩余的混合物].
请回答:
(1)双氧水样品中加入二氧化锰,二氧化锰起催化作用,反应生成氧气的物质的量为0.8g.
(2)计算该过氧化氢溶液中溶质的质量分数.(写出计算过程)
(3)实验装置中锥形瓶上加接盛有碱石灰的干燥管作用是吸收装置内向外跑的水蒸汽.如果实验装置中不接盛有碱石灰的干燥管,测得的过氧化氢溶液溶质的质量分数会偏大,原因是如果实验装置中不接盛有碱石灰的干燥管,导致装置内一些水蒸气跑掉,质量减少的多了,算出来的氧气的质量大了,所以算出来的过氧化氢质量偏大,测得的过氧化氢溶液溶质的质量分数会偏大.
分析 根据装置的质量的减少量就是生成氧气的质量,由于过氧化氢中水分容易向空气中扩散加上干燥剂进行吸收,再进一步进行分析即可.
解答 解:(1)催化剂所起的作用叫做催化作用,根据质量守恒定律可知,装置的质量的减少量就是生成氧气的质量,所以生成氧气的质量:84g+0.5g-83.7g=0.8g.
(2)设要生成0.8g氧气需要参加反应的过氧化氢的质量为X则:
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 0.8g
$\frac{68}{x}=\frac{32}{0.8g}$
解得x=1.7g,过氧化氢溶液质量为:84g-16g=68g,所以过氧化氢溶液中溶质的质量分数=$\frac{1.7g}{68g}$×100%=2.5%;
(3)实验装置中锥形瓶上加接盛有碱石灰的干燥管作用是吸收装置内向外跑的水蒸汽,如果实验装置中不接盛有碱石灰的干燥管,则如果实验装置中不接盛有碱石灰的干燥管,导致装置内一些水蒸气跑掉,质量减少的多了,算出来的氧气的质量大了,所以算出来的过氧化氢质量偏大,测得的过氧化氢溶液溶质的质量分数会偏大.
故答案为:
(1)催化;0.8g;
(2)2.5%;
(3)吸收装置内向外跑的水蒸汽;如果实验装置中不接盛有碱石灰的干燥管,导致装置内一些水蒸气跑掉,质量减少的多了,算出来的氧气的质量大了,所以算出来的过氧化氢质量偏大,测得的过氧化氢溶液溶质的质量分数会偏大.
点评 本题主要考查化学方程式的书写和有关化学方程式的计算,难度较小.

练习册系列答案
相关题目
9.“慈母手中线,游子身上衣”.棉花的主要成分是纤维素[(C6H10O5)n].下列说法不正确的是( )
| A. | 纤维素是由C、H、O三种元素组成的 | |
| B. | 棉线与羊毛线可用燃烧的方法区别 | |
| C. | 纤维素中C、H、O三种元素的原子个数比为6:10:5 | |
| D. | 纤维素中C、H、O三种元素的质量比为12:1:16 |
8.下列属于纯净物的是( )
| A. | 碘酒 | B. | 食醋 | C. | 软水 | D. | 金刚石 |
9.下列说法属于化学性质的是( )
| A. | 铝能导电 | B. | 金刚石硬度最大 | ||
| C. | 氧气常温下呈气态 | D. | 铁钉会生锈 |
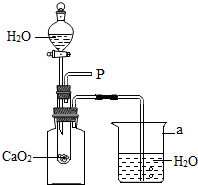 小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.
小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.