题目内容
16.现欲探究一固体混合物A的成分,已知其中可能含有CuCl2、CaCO3、NaCl、Mg,四种物质中的两种或多种.按图所示进行实验.出现的现象如图中所述(设过程中所有可能发生的反应都恰好完全进行).
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)固体D的颜色为红色;
(2)溶液C中的溶质是(写化学式)CaCl2、MgCl2;
(3)混合物A中,肯定存在的物质是(写化学式)Mg、CaCO3、CuCl2;
(4)写出实验过程②中生成沉淀G所发生反应的化学方程式:CO2+Ca(OH)2=CaCO3↓+H2O.
分析 根据固体混合物与稀盐酸混合生成使澄清石灰水变浑浊的气体B,所以气体B是二氧化碳,混合物中一定含有含有碳酸钙,固体D和硝酸银反应会生成固体B和溶液F,所以固体D是铜,混合物中一定含有氯化铜和镁,镁和盐酸会生成氯化镁和氢气,碳酸钙和盐酸会生成氯化钙、水和二氧化碳,然后结合题中的现象进行分析.
解答 解:固体混合物与稀盐酸混合生成使澄清石灰水变浑浊的气体B,所以气体B是二氧化碳,混合物中一定含有含有碳酸钙,固体D和硝酸银反应会生成固体B和溶液F,所以固体D是铜,混合物中一定含有氯化铜和镁,镁和盐酸会生成氯化镁和氢气,碳酸钙和盐酸会生成氯化钙、水和二氧化碳,所以
(1)固体D的颜色为红色;
(2)溶液C中的溶质是:CaCl2、MgCl2;
(3)混合物A中,肯定存在的物质是:Mg、CaCO3、CuCl2;
(4)实验过程②中生成沉淀G所发生的反应是二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.
故答案为:(1)红;
(2)CaCl2、MgCl2;
(3)Mg、CaCO3、CuCl2;
(4)CO2+Ca(OH)2=CaCO3↓+H2O.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
6.积累与运用是化学学习的基础,下面是这学期张伟同学整理的部分化学知识,其中正确的是( )
| A. | 构成物质的基本粒子:分子、原子、离子 | |
| B. | 常见的可燃性气体:氢气、一氧化碳、天然气(主要成分甲烷)4 | |
| C. | 常见的合金:硬铝、青铜、氧化铁 | |
| D. | 溶于水放热的物质:氢氧化钠固体、食盐固体、硝酸铵固体 |
7.下列物质的化学式和相应的名称都正确的是( )
| A. | O3 氧气 | B. | MgCl2 氯化镁 | C. | AlO氧化铝 | D. | FeSO4硫酸铁 |
11.带火星的木条在氧气中可以复燃.那么,是不是只有纯净的氧气才能使带火星的木条复燃呢?为此,同学们开展了相关探究实验.实验主要步骤如下:先制取一定量的氧气备用,再测得集气瓶实际容积为317毫升,然后采用某种方法得到5瓶含氧量不同的空气,最后用带火星的木条来试验,观察是否复燃.相关的数据见下表:
(1)表空白处的数值为45.2% (保留1位小数);
(2)由该实验可得到的结论是空气中氧气体积分数大于或等于41.9%时,能使带火星的木条复燃.
| 集气瓶编号 | 瓶内预装水 体积/毫升 | 充入氧气 体积/毫升 | 瓶内空气 体积/毫升 | 瓶内空气里氧气 体积的百分比 | 木条能否复燃 |
| 1 | 120 | 120 | 197 | 50.9% | 能 |
| 2 | 97 | 97 | 220 | 45.2% | 能 |
| 3 | 90 | 90 | 227 | 43.4% | 能 |
| 4 | 84 | 84 | 233 | 41.9% | 能 |
| 5 | 81 | 81 | 236 | 41.2% | 不能 |
(2)由该实验可得到的结论是空气中氧气体积分数大于或等于41.9%时,能使带火星的木条复燃.
1.下列反应的生成物全部为氧化物的分解反应是( )
| A. | 氯酸钾和二氧化锰共热 | B. | 铜绿受热 | ||
| C. | 甲烷燃烧 | D. | 氧化汞受热分解 |
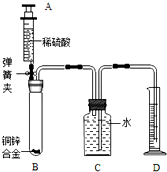 某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)探究过程如下:
某化学小组利用下图所示装置测定铜锌合金样品中锌的质量分数(图中固定装置已略去)探究过程如下: .
. 某同学按如图所示的装置进行实验:将浸有酚酞溶液的棉花团绑在树形铁丝上制成“花树”,在玻璃片上放置盛有浓氨水的微型烧杯,罩上大烧杯.
某同学按如图所示的装置进行实验:将浸有酚酞溶液的棉花团绑在树形铁丝上制成“花树”,在玻璃片上放置盛有浓氨水的微型烧杯,罩上大烧杯.