题目内容
6. 如图是A、B、C三种固体物质的溶解度曲线,下列说法错误的是( )
如图是A、B、C三种固体物质的溶解度曲线,下列说法错误的是( )| A. | t1℃时,溶解度最大的物质是B | |
| B. | 在t2℃时,把150g A物质的饱和溶液降温到t1℃,析出晶体的质量为25g | |
| C. | t2℃时A、B、C三种物质的混合溶液100克,恒温蒸发,先析出的晶体一定是C | |
| D. | 用同一种方法可以使A、B、C三种物质的溶液都有晶体析出,该方法是蒸发结晶 |
分析 A、根据溶解度曲线可比较溶解度大小;
B、根据不同温度下的溶解度分析析出晶体质量;
C、不知溶液中各溶质的质量多少,无法判断哪种物质先析出晶体;
D、根据溶解度曲线分析结晶方法.
解答 解:A、由溶解度曲线可知t1℃时溶解度最大的是B,正确;
B、在t2℃时A的溶解度是50g,即100g水中最多溶解50g的A,则150g A物质的饱和溶液中有50g的A,降温到t1℃溶解度变为25g,因此析出晶体的质量为25g,正确;
C、不知溶液中各溶质的质量多少,无法判断哪种物质先析出晶体;故错误;
D、ABC的溶液均可用蒸发溶剂的方法使其析出晶体,正确;
故选:C.
点评 本题综合考查溶解度曲线的意义,要求我们灵活掌握溶解概念,同时明确对于不同种类的物质均可可以采用蒸发结晶的方法.

练习册系列答案
相关题目
16.某校化学小组对热水壶底部水垢的主要成分进行了如下探究,请完成以下活动并回答相关问题.
【查阅资料】
天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见下表(20℃):
根据上述物质的溶解性,小组同学确定水垢的主要成分中一定含有的两种物质是,可能含有Ca(OH)2和MgCO3.
【提出问题】水垢的主要成分中是否含有Ca(OH)2和MgCO3呢?
【实验方案1】确定水垢中是否含Ca(OH)2
【实验方案2】确定水垢中是否含MgCO3
利用下列实验装置,完成实验2探究.其主要实验步骤如下:
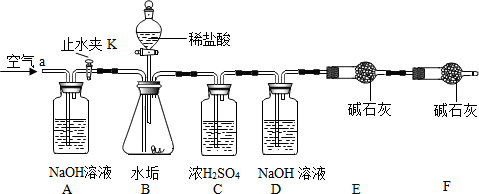
按如图组装后,将9.8g水垢试样放入锥形瓶中,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后精确称量D、E装置总质量为600.0g关闭止水夹K,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处再次缓缓鼓入空气,一段时间后称量装置D、E的总质量为604.4g(注意:碱石灰主要成分为CaO和NaOH的混合物).
【实验讨论】
(1)加入药品前应;待锥形瓶中不再产生气泡时,打开止水夹K,缓缓鼓入空气的目的是.
(2)C装置的作用是:干燥生成的气体.
(3)装置 B中生成CO2的质量为4.4g.通过计算说明该水垢中(填序号)含MgCO3.
A.一定B.一定不C.可能D.无法确定
【实验方案3】定量探究水垢中氢氧化镁的质量分数
另取质量为9.8g的水垢试样,加入7.3%稀盐酸与之恰好完全反应,测得消耗稀盐酸110g.结合以上数据和实验结论,计算水垢样品中氢氧化镁的质量分数(写出计算过程,结果保留1位小数).
【反思】缺少F装置会使所测水垢样品中氢氧化镁的质量分数偏小(填写“偏大”或“偏小”或“不变”).
【查阅资料】
天然水中含有Ca2+、Mg2+、HCO3-等离子,在加热条件下,这些离子趋于生成溶解度更小的物质--水垢(主要成分为碳酸盐和碱).有关物质的溶解性见下表(20℃):
| 阴离子 阳离子 | OH- | CO32- | HCO3- |
| Ca2+ | 微溶 | 不溶 | 可溶 |
| Mg2+ | 不溶 | 微溶 | 可溶 |
【提出问题】水垢的主要成分中是否含有Ca(OH)2和MgCO3呢?
【实验方案1】确定水垢中是否含Ca(OH)2
| 实验步骤 | 实验现象 | 结论 |
| 在少量研碎的水垢中,加入适量的蒸馏水充分搅拌,过滤,在滤液里加入Na2CO3溶液. | 无白色沉淀 | 水垢中无Ca(OH)2 |
利用下列实验装置,完成实验2探究.其主要实验步骤如下:

按如图组装后,将9.8g水垢试样放入锥形瓶中,打开止水夹K,从导管a处缓缓鼓入空气,一段时间后精确称量D、E装置总质量为600.0g关闭止水夹K,加入足量稀盐酸溶液,待锥形瓶中不再产生气泡时,打开止水夹K,从导管a处再次缓缓鼓入空气,一段时间后称量装置D、E的总质量为604.4g(注意:碱石灰主要成分为CaO和NaOH的混合物).
【实验讨论】
(1)加入药品前应;待锥形瓶中不再产生气泡时,打开止水夹K,缓缓鼓入空气的目的是.
(2)C装置的作用是:干燥生成的气体.
(3)装置 B中生成CO2的质量为4.4g.通过计算说明该水垢中(填序号)含MgCO3.
A.一定B.一定不C.可能D.无法确定
【实验方案3】定量探究水垢中氢氧化镁的质量分数
另取质量为9.8g的水垢试样,加入7.3%稀盐酸与之恰好完全反应,测得消耗稀盐酸110g.结合以上数据和实验结论,计算水垢样品中氢氧化镁的质量分数(写出计算过程,结果保留1位小数).
【反思】缺少F装置会使所测水垢样品中氢氧化镁的质量分数偏小(填写“偏大”或“偏小”或“不变”).
15.以下实验的实验现象描述,正确的是( )
| A. | 久置于空气中的熟石灰,加入足量稀盐酸无气体产生 | |
| B. | 硫酸铜溶液中滴入氢氧化钠溶液,有蓝色沉淀生成 | |
| C. | 分别点燃一小块棉纤维和羊毛纤维,都有烧焦羽毛的气味 | |
| D. | 氯化铵固体和熟石灰混合研磨,生成无色无味的气体 |
16.2014年11月,APEC会议在北京召开.会议期间,久违的蓝天白云在北京重现.要想让“APEC蓝”变成“持续蓝”,下列做法不应提倡的是( )
| A. | 车辆限行 | B. | 污染企业停工整治 | ||
| C. | 植树造林 | D. | 燃煤发电 |
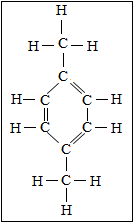 2015年4月6日位于福建漳州的PX项目突然起火爆炸引起世人关注.PX学名对二甲苯,其组成和结构如图所示.PX来自石油制品,主要用于制取生产涤纶纤维的原料聚酯树脂.
2015年4月6日位于福建漳州的PX项目突然起火爆炸引起世人关注.PX学名对二甲苯,其组成和结构如图所示.PX来自石油制品,主要用于制取生产涤纶纤维的原料聚酯树脂.