题目内容
1.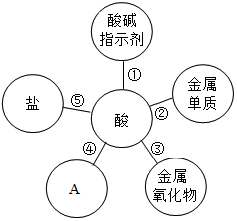 归纳是学习的重要方法,小红在复习硫酸和盐酸的性质时归纳出硫酸和盐酸的五条化学性质(如右图所示,连线表示相互反应).
归纳是学习的重要方法,小红在复习硫酸和盐酸的性质时归纳出硫酸和盐酸的五条化学性质(如右图所示,连线表示相互反应).(1)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是浓盐酸.
(2)它们都能除铁锈,写出盐酸与铁锈主要成分反应的化学方程式Fe2O3+6HCl═2FeCl3+3H2O.
(3)请写出把硫酸转变为盐酸的化学方程式BaCl2+H2SO4═BaSO4↓+2HCl.
分析 (1)浓硫酸具有吸水性,浓盐酸具有挥发性;
(2)铁锈的主要成分是氧化铁,氧化铁和稀盐酸反应生成氯化铁和水;
(3)氯化钡和稀硫酸反应生成硫酸钡沉淀和盐酸.
解答 解:(1)打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶时,盛有浓硫酸的试剂瓶无明显现象,盛有浓盐酸的试剂瓶口出现白雾,这是因为浓盐酸挥发出的氯化氢在瓶口处与水蒸气结合成了盐酸小液滴.故填:浓盐酸.
(2)盐酸与铁锈主要成分反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O.故填:Fe2O3+6HCl═2FeCl3+3H2O.
(3)硫酸转变为盐酸的化学方程式为:BaCl2+H2SO4═BaSO4↓+2HCl.故填:BaCl2+H2SO4═BaSO4↓+2HCl.
点评 酸具有一些相似的化学性质,例如能使石蕊试液变红色,能和某些金属单质、某些金属氧化物、某些盐、碱反应生成相应的物质.

练习册系列答案
相关题目
11.能保持氢气化学性质的微粒的是( )
| A. | 氢元素 | B. | 氢原子 | C. | 氢离子 | D. | 氢分子 |
9.下列除杂质的方法错误的是( )
| 选项 | 物质(括号内为杂质) | 除杂方法 |
| A | NaCl(泥沙) | 溶解、过滤、蒸发 |
| B | CO2(CO) | 通入澄清石灰水 |
| C | FeCl2(CuCl2) | 加入适量铁粉 |
| D | CaCl2溶液(盐酸) | 加入过量CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
16. 下面右图中,四圆甲、乙、丙、丁分别表示一种溶液,两圆的相交部分为两溶液混合后出现的主要实验现象,表中符合图示关系的是( )
下面右图中,四圆甲、乙、丙、丁分别表示一种溶液,两圆的相交部分为两溶液混合后出现的主要实验现象,表中符合图示关系的是( )
 下面右图中,四圆甲、乙、丙、丁分别表示一种溶液,两圆的相交部分为两溶液混合后出现的主要实验现象,表中符合图示关系的是( )
下面右图中,四圆甲、乙、丙、丁分别表示一种溶液,两圆的相交部分为两溶液混合后出现的主要实验现象,表中符合图示关系的是( )| 甲 | 乙 | 丙 | 丁 | |
| A | Na2CO3 | H2SO4 | Ba(OH)2 | 石蕊 |
| B | Na2CO3 | HCl | Ca(OH)2 | CuSO4 |
| C | Na2SO4 | HCl | Ba(OH)2 | 石蕊 |
| D | HCl | Na2CO3 | Ca(OH)2 | 酚酞 |
| A. | A | B. | B | C. | C | D. | D |
13.利用摄影店废弃的定影液,每月可回收价值较高的银.一种回收方法的反应原理是:Fe+2AgNO3=2Ag+Fe(NO3)2,这个反应属于( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
10.实验室在向40克氧化铁粉末中通氢气使其充分反应,用制得的铁与硫酸反应制取硫酸亚铁晶体.要使40克氧化铁完全被还原,需要氢气的质量是( )
| A. | 1.5克 | B. | 少于1.5克 | C. | 多于1.5克 | D. | 不多于1.5克 |
11.下列实验方案能证明铁、铜、银三种金属活动性顺序的是( )
| A. | 将铁丝、铜丝分别放入硝酸银溶液中,根据现象,判断结果 | |
| B. | 将铁丝分别放入硫酸铜、硝酸银溶液中,根据现象,判断结果 | |
| C. | 将铁、铜、银三种金属丝分别放入稀硫酸中,根据现象,判断结果 | |
| D. | 将铜丝分别放入硝酸银、硝酸亚铁溶液中,根据现象,判断结果 |
