题目内容
10.实验室在向40克氧化铁粉末中通氢气使其充分反应,用制得的铁与硫酸反应制取硫酸亚铁晶体.要使40克氧化铁完全被还原,需要氢气的质量是( )| A. | 1.5克 | B. | 少于1.5克 | C. | 多于1.5克 | D. | 不多于1.5克 |
分析 根据氧化铁与足量氢气充分反应的化学方程式和氧化铁的质量,列出比例式,就可计算出需要氢气的质量.根据反应开始需要通一段时间的氢气将玻璃管内空气排净、实验结束后要继续通入氢气直到试管冷却进行分析.
解答 解:设理论上需要氢气的质量为x,则
3H2+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O
6 160
x 40g
$\frac{6}{160}=\frac{x}{40g}$
x=1.5g
反应开始需要通一段时间的氢气将玻璃管内的空气排净,防止氢气和空气的混合气加热发生爆炸,实验结束后要继续通入氢气以防铁被重新氧化,所以若要还原40g氧化铁,需要氢气的质量大于1.5g.
故选C.
点评 本题主要考查学生运用化学方程式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
20.下列各组物质,都属于同一类物质(按单质、酸、碱、盐、氧化物分类)的是( )
| A. | 生石灰、熟石灰、烧碱 | B. | 氧化钠、生石灰、干冰 | ||
| C. | 硫酸铝、碳酸钙、石灰水 | D. | 氯气、钡、磷酸 |
5.在20℃时,氯化钠的溶解度是36克.在20℃时,把20克氯化钠投入50克水中,充分溶解后,下列有关说法不正确的是( )
| A. | 制成70克饱和溶液 | B. | 制成68克饱和溶液 | ||
| C. | 有18克氯化钠发生溶解 | D. | 还剩余2克固体氯化钠未溶解 |
2.在盛有AgNO3和Mg(NO3)2混合溶液的试管中,加入一定量的锌粉充分反应,试管底部有少量固体存在.过滤,向滤液中加稀盐酸,产生白色沉淀,滤渣是( )
| A. | Mg | B. | Ag | C. | Zn 和Ag | D. | Zn 和Mg |
19.下列化肥中属于复合肥料的是( )
| A. | NH4NO3 | B. | KCl | C. | KNO3 | D. | Ca3(PO4)2 |
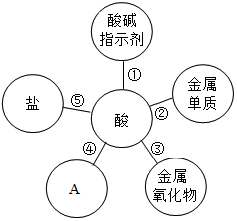 归纳是学习的重要方法,小红在复习硫酸和盐酸的性质时归纳出硫酸和盐酸的五条化学性质(如右图所示,连线表示相互反应).
归纳是学习的重要方法,小红在复习硫酸和盐酸的性质时归纳出硫酸和盐酸的五条化学性质(如右图所示,连线表示相互反应). 如图是浓盐酸试剂瓶上标签的部分内容,请回答:该浓盐酸的溶质名称是氯化氢,现要配制3%的稀盐酸120g,需要这种浓盐酸10g,使用一段时间后浓盐酸质量分数小于36%.其原因是浓盐酸具有挥发性.
如图是浓盐酸试剂瓶上标签的部分内容,请回答:该浓盐酸的溶质名称是氯化氢,现要配制3%的稀盐酸120g,需要这种浓盐酸10g,使用一段时间后浓盐酸质量分数小于36%.其原因是浓盐酸具有挥发性.