题目内容
钢铁是人类生产生活中应用最广泛的金属材料,请回答下列与此有关的问题.
(1)酸菜等酸性的食物不宜用铁制器具长期盛放,因为
(2)铁、铝、铜是我们生产生活中使用比较广泛的金属,如图所示用品中,利用金属导热性的是 ,延展性的是 (填字母序号)

(3)对铁“发蓝”处理,其表面将形成致密氧化膜而有效避免腐蚀.
①“发蓝”过程的化学方程式如下,式中X的化学式为
36Fe+4NaNO2+9NaNO3+26H2O═12X+13NaOH+13NH3↑
②为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质,由此可知该零件“发蓝”处理效果 (填“好”或“不好”),因为 (用化学方程式表示)
(1)酸菜等酸性的食物不宜用铁制器具长期盛放,因为
(2)铁、铝、铜是我们生产生活中使用比较广泛的金属,如图所示用品中,利用金属导热性的是

(3)对铁“发蓝”处理,其表面将形成致密氧化膜而有效避免腐蚀.
①“发蓝”过程的化学方程式如下,式中X的化学式为
36Fe+4NaNO2+9NaNO3+26H2O═12X+13NaOH+13NH3↑
②为检验“发蓝”处理的铁质零件表面是否形成致密氧化膜,将该零件浸泡于硫酸铜溶液中,发现零件表面出现红色物质,由此可知该零件“发蓝”处理效果
考点:金属的化学性质,金属的物理性质及用途,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)根据铁能与酸反应进行分析;
(2)根据物质的用途分析物质的性质;
(3)①根据质量守恒定律进行分析;
②根据铁能与硫酸铜反应生成硫酸亚铁和铜,可观察到铁丝表面出现红色固体,溶液由蓝色逐渐变为无色进行分析.
(2)根据物质的用途分析物质的性质;
(3)①根据质量守恒定律进行分析;
②根据铁能与硫酸铜反应生成硫酸亚铁和铜,可观察到铁丝表面出现红色固体,溶液由蓝色逐渐变为无色进行分析.
解答:解:(1)铁的活动性在H的前面,能与酸反应,所以酸菜等酸性的食物不宜用铁质器具长期盛放;
(2)通过分析物质的用途可知,利用金属导热性的是A,延展性的是BC;
(3)①根据质量守恒定律,反应前后原子的种类和数目不变,反应前:Fe原子数目为36,Na原子的数目为13,N原子的数目为13,O原子的数目为57,H原子的数目为52;反应后:Fe原子数目为0,Na原子的数目为13,N原子的数目为13,O原子的数目为13,H原子的数目为52;所以X的化学式为:Fe3O4;
②如果氧化膜不致密,裸露出来的铁与硫酸铜的反应生成了铜和硫酸亚铁,反应的方程式为Fe+CuSO4 ═FeSO4 +Cu.
故答案为:(1)铁会与酸性物质反应而被腐蚀;
(2)A,BC;
(3)①Fe3O4;
②不好,Fe+CuSO4=Cu+FeSO4.
(2)通过分析物质的用途可知,利用金属导热性的是A,延展性的是BC;
(3)①根据质量守恒定律,反应前后原子的种类和数目不变,反应前:Fe原子数目为36,Na原子的数目为13,N原子的数目为13,O原子的数目为57,H原子的数目为52;反应后:Fe原子数目为0,Na原子的数目为13,N原子的数目为13,O原子的数目为13,H原子的数目为52;所以X的化学式为:Fe3O4;
②如果氧化膜不致密,裸露出来的铁与硫酸铜的反应生成了铜和硫酸亚铁,反应的方程式为Fe+CuSO4 ═FeSO4 +Cu.
故答案为:(1)铁会与酸性物质反应而被腐蚀;
(2)A,BC;
(3)①Fe3O4;
②不好,Fe+CuSO4=Cu+FeSO4.
点评:本题考查的是金属活动顺序表的应用及金属的锈蚀等,要能应用必须先把金属活动顺序表熟练的掌握住.金属的知识是重要的内容,应加强学习.

练习册系列答案
相关题目
下列化学符号既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A、O |
| B、Cu |
| C、C60 |
| D、H2 |
可以判断溶液一定呈酸性的是( )
| A、滴加酚酞试液显红色的溶液 |
| B、滴加石蕊试液显蓝色的溶液 |
| C、能够与碱发生反应的溶液 |
| D、常温下,pH<7的溶液 |
有X,Y,Z三种金属,如果把它们分别放入稀硫酸中,X表面有气泡产生,Y,Z无变化,如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化,根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为( )
| A、X>Y>Z |
| B、Z>Y>Z |
| C、Y>X>Z |
| D、Y>Z>X |
将一杯20℃时的硝酸钠饱和溶液变为不饱和溶液,可采用的方法是( )
| A、加入溶剂 | B、升高温度 |
| C、降低温度 | D、蒸发溶剂 |
下图所示实验基本操作错误的是( )
A、 倾倒液体 |
B、 读取液体体积 |
C、 检查气密性 |
D、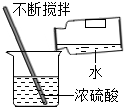 稀释浓硫酸 |
 “低碳生活,绿色出行”,如图为某自行车的结构,请回答下列问题:
“低碳生活,绿色出行”,如图为某自行车的结构,请回答下列问题: A、B、C三种固体物质的溶解度曲线如图所示,据图完成下列问题:
A、B、C三种固体物质的溶解度曲线如图所示,据图完成下列问题: