题目内容
12.通过一年的化学学习,相信你已掌握了实验室制取气体的有关知识,请结合图示回答下列问题.
(1)实验室常用过氧化氢溶液和二氧化锰混合制取氧气,发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,选用的发生装置是A,(填装置序号,下同)收集装置是B或D.
(2)常温常压下一氧化碳不与空气反应,但因密度很接近空气而不用排空气法收集.若用排空气收集一氧化碳,将不易排尽瓶内空气,导致收集到的气体不纯;排水法收集一氧化碳时,待导气管口有连续稳定的冒出气泡才开始收集,原因是防止收集到的气体因混有空气而不纯.
分析 (1)实验室常用过氧化氢溶液和二氧化锰混合制取氧气,属于固液常温型,根据氧气的密度及水溶性来选择收集装置.
(2)根据常温常压下一氧化碳不与空气反应,但因密度很接近空气儿不用排空气法收集,结合收集时的注意事项,进行分析解答.
解答 解:(1)实验室常用过氧化氢溶液和二氧化锰混合制取氧气,反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;属于固液常温型,选用的发生装置是A;氧气不易溶于水,密度比空气的大,能用排水法、向上排空气法收集,即收集装置是B或D.
(2)常温常压下一氧化碳不与空气反应,但因密度很接近空气儿不用排空气法收集.一氧化碳的密度与空气接近,若用排空气收集一氧化碳,将不易排尽瓶内空气,导致收集到的气体不纯.
排水法收集一氧化碳时,待导气管口有连续稳定的冒出气泡才开始收集,原因是刚开始排出的是空气,会导致收集到的气体因混有空气而不纯.
故答案为:(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;A;B或D;(2)不易排尽瓶内空气,导致收集到的气体不纯;(3)防止收集到的气体因混有空气而不纯.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取气体的反应原理、发生装置和收集装置的选择依据等是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.控制变量法是科学探究中常用的方法之一.
(1)在探究固体物质的溶解度时,需要考虑的因素有:①溶质的种类;②溶剂的种类;③溶质最多被溶解的质量;④溶剂的质量;⑤温度.
如测定“某物质在不同温度下的溶解度”,研究的是③(填序号)受温度的影响,这就需要控制其他因素保持不变.
(2)右表是利用控制变量法测得的氯化钠、硝酸钾在不同温度时的溶解度,请根据表格内容及实验现象回答下列问题.
①从上表可知,两种物质的溶解度受温度变化影响较大的是硝酸钾;
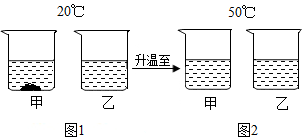
②20℃时,将等质量的NaCl、KNO3分别放入盛有100g水的两个烧杯中,充分溶解后如图1所示,升温到50℃时如图2所示.试判断:50℃时甲烧杯中的溶液一定是不饱和溶液(填“饱和溶液”、“不饱和溶液”或“不能确定”).
(1)在探究固体物质的溶解度时,需要考虑的因素有:①溶质的种类;②溶剂的种类;③溶质最多被溶解的质量;④溶剂的质量;⑤温度.
如测定“某物质在不同温度下的溶解度”,研究的是③(填序号)受温度的影响,这就需要控制其他因素保持不变.
(2)右表是利用控制变量法测得的氯化钠、硝酸钾在不同温度时的溶解度,请根据表格内容及实验现象回答下列问题.
| 温度(℃) | 20 | 40 | 50 | |
| 溶解度/g | NaCl | 36.0 | 36.6 | 37.0 |
| KNO3 | 31.6 | 63.9 | 85.5 | |
②20℃时,将等质量的NaCl、KNO3分别放入盛有100g水的两个烧杯中,充分溶解后如图1所示,升温到50℃时如图2所示.试判断:50℃时甲烧杯中的溶液一定是不饱和溶液(填“饱和溶液”、“不饱和溶液”或“不能确定”).

17.空气是人类的宝贵资源,下列有关空气的说法错误的是(( )
| A. | 空气的成分按体积计算,含量最多的气体是氮气 | |
| B. | 空气是混合物 | |
| C. | 氧气具有可燃性 | |
| D. | 稀有气体的化学性质不活泼 |
4.遇到火灾时,正确处理火险有利于保护生命财产安全,下列处理方式中错误的是( )
| A. | 如果是室内着火,立即打开所有门窗 | |
| B. | 用湿毛巾捂住口鼻,蹲下靠近地面.迅速离开火灾现场 | |
| C. | 发现火灾立即拨打119火警电话 | |
| D. | 炒菜时油锅着火,立即盖上锅盖 |
2.下列物质在pH=1的溶液中能大量共存,且溶液为无色的是( )
| A. | NH4Cl、Na2SO4、KNO3 | B. | NaCl、Na2CO3、Na2SO4 | ||
| C. | BaCl2、K2SO4、NaOH | D. | FeCl3、Ba(NO3)2、CaCl2 |
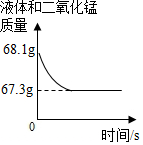 化学兴趣小组用一瓶久置的过氧化氢溶液制取氧气并测量过氧化氢质量分数.称量 68g 过氧化氢溶液和 0.1g 二氧化锰进行实验,反应前后质量随时间变化关系如图.计算:
化学兴趣小组用一瓶久置的过氧化氢溶液制取氧气并测量过氧化氢质量分数.称量 68g 过氧化氢溶液和 0.1g 二氧化锰进行实验,反应前后质量随时间变化关系如图.计算:

 A、B、C、D、E、F是初中化学常见的六种物质,已知A是一种单质,B为红棕色固体,D常用于改良酸性土壤,F与B属于同类物质,其相互反应情况如图所示(短线“一”相连的物质间能反应,箭头“→”表示能生成).
A、B、C、D、E、F是初中化学常见的六种物质,已知A是一种单质,B为红棕色固体,D常用于改良酸性土壤,F与B属于同类物质,其相互反应情况如图所示(短线“一”相连的物质间能反应,箭头“→”表示能生成).