题目内容
3.某化学兴趣小组的同学做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50g5%的氯化钠溶液.实验一:如图是同学们做粗盐提纯实验的操作示意图.
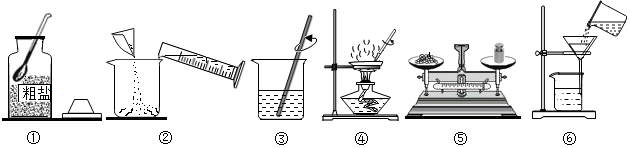
请回答下列问题:
(1)操作③中用玻璃棒搅拌的作用是搅拌,加快溶解速率.
(2)操作⑥中的错误是没有用玻璃棒引流.
(3)粗盐提纯实验的操作顺序为(填操作序号)①⑤②③⑥④、称量精盐并计算产率.
分析 (1)操作③是溶解操作,据此进行分析解答.
(2)过滤液体时,注意“一贴、二低、三靠”的原则.
(3)根据粗盐提纯是将粗盐中含有的泥沙等不溶物除去,进行分析解答.
解答 解:(1)操作③是溶解操作,玻璃棒搅拌的作用是搅拌,加快溶解速率.
(2)过滤液体时,要注意“一贴、二低、三靠”的原则,图中没有用玻璃棒引流.
(3)首先称量粗盐的质量,粗盐的主要成分是氯化钠,粗盐提纯是通过溶解(把不溶物与食盐初步分离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐)得到精盐的过程,操作顺序为①⑤②③⑥④、称量精盐并计算产率.
故答案为:(1)搅拌,加快溶解速率;(2)没有用玻璃棒引流;(3)①⑤②③⑥④.
点评 本题难度不大,掌握粗盐提纯的原理、过滤的注意事项等并能灵活运用是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16. 下图为xx泡打粉的标签如图所示,下列说法错误的是( )
下图为xx泡打粉的标签如图所示,下列说法错误的是( )
 下图为xx泡打粉的标签如图所示,下列说法错误的是( )
下图为xx泡打粉的标签如图所示,下列说法错误的是( )| A. | 碳酸氢钠俗称小苏打 | B. | 泡打粉可以随意放置 | ||
| C. | 加入泡打粉制作的蛋糕更松软 | D. | 面粉是有机物,碳酸盐是无机物 |
17.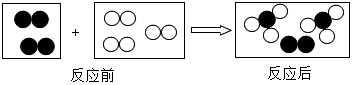 如图是某化学反应的微观模型,“
如图是某化学反应的微观模型,“ ”、“
”、“ ”分别表示不同元素的原子.下列对图示模型理解正确的是( )
”分别表示不同元素的原子.下列对图示模型理解正确的是( )
 如图是某化学反应的微观模型,“
如图是某化学反应的微观模型,“ ”、“
”、“ ”分别表示不同元素的原子.下列对图示模型理解正确的是( )
”分别表示不同元素的原子.下列对图示模型理解正确的是( )| A. | 生成物的化学式可能是NH3 | |
| B. | 该反应有单质生成 | |
| C. | 该反应属于复分解反应 | |
| D. | 参加反应的两种物质分子个数之比为2:3 |
14.下列实验操作正确的是( )
| A. | 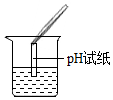 测定末知溶液的pH | B. | 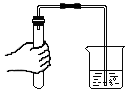 检査装置气密性 | ||
| C. | 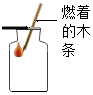 检验CO2 | D. |  称量食盐 |
8.如表为氯化钠和氯化铵在不同温度时的溶解度,请回答下列问题
(1)由表中数据可知,溶解度随温度变化较大的物质是氯化铵;
(2)20℃时,100g水最多能溶解NaCl36.0g.
(3)向烧杯中加入100g水和49.0g氯化铵配成50℃的溶液,此时溶液为不饱和溶液(填“饱和”或“不饱和”);再冷却到20℃,烧杯中析出固体的质量为11.8g.
另外多角度看物质,有助于加深对物质的认识.Na2CO3是一种常见的盐,请回答:
(4)Na2CO3溶液显碱性,其pH>7(填“<”、“>”或“=”).
(5)Na2CO3可看成是碱和氧化物反应的产物,写出反应的化学方程式2NaOH+CO2═Na2CO3+H2O.
(6)Na2CO3作为反应物之一,写出一个符合A+B→C+D形成的化学方程式CaCl2+Na2CO3═CaCO3↓+2NaCl.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 |
| NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 49.6 |
| NaCl溶解度/g | 35.4 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
(2)20℃时,100g水最多能溶解NaCl36.0g.
(3)向烧杯中加入100g水和49.0g氯化铵配成50℃的溶液,此时溶液为不饱和溶液(填“饱和”或“不饱和”);再冷却到20℃,烧杯中析出固体的质量为11.8g.
另外多角度看物质,有助于加深对物质的认识.Na2CO3是一种常见的盐,请回答:
(4)Na2CO3溶液显碱性,其pH>7(填“<”、“>”或“=”).
(5)Na2CO3可看成是碱和氧化物反应的产物,写出反应的化学方程式2NaOH+CO2═Na2CO3+H2O.
(6)Na2CO3作为反应物之一,写出一个符合A+B→C+D形成的化学方程式CaCl2+Na2CO3═CaCO3↓+2NaCl.
13.苯酚(化学式为C6H6O)是一种重要的有机化合物,是生产某些树脂、杀菌剂、防腐剂以及药物(如阿司匹林)的重要原料.下列关于苯酚的叙述正确的是( )
| A. | 苯酚是由6个碳原子、6个氢原子和1个氧原子构成 | |
| B. | 苯酚是由碳、氢、氧三种元素组成的,但它不属于氧化物 | |
| C. | 苯酚中,碳、氢、氧元素的质量比为6:6:1 | |
| D. | 苯酚中,氧元素的质量分数最小 |
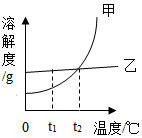 如图为甲、乙两种固体物质的溶解度曲线,请据图回答下列问题
如图为甲、乙两种固体物质的溶解度曲线,请据图回答下列问题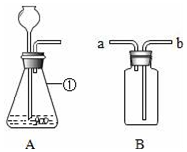 通过一年的化学学习,你已经掌握了实验室制取气体的有关方法.请根据图回答问题:
通过一年的化学学习,你已经掌握了实验室制取气体的有关方法.请根据图回答问题: