题目内容
1. (1)如图是a、b、c三种物质溶解度曲线,a与c溶解度曲线相交于P点.据图回答:①P点的含义是当温度为t1℃时,a与c的溶解度相等.
(1)如图是a、b、c三种物质溶解度曲线,a与c溶解度曲线相交于P点.据图回答:①P点的含义是当温度为t1℃时,a与c的溶解度相等.②t2℃时30g a物质加入到50g水中不断搅拌,形成溶液质量是75g.
③将t2℃时a、b、c三种物质饱和溶液的温度降到t1℃时,三种溶液中溶质的质量分数由大到小的顺序排列是b>a>c
(2)KNO3和KCl在不同温度时的溶解度如下表所示:
| /℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| /g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
分析 (1)①溶解度曲线的交点表示该温度下二者的溶解度相等;
②据该温度下a的溶解度分析解答;
③饱和溶液中溶质的质量分数═$\frac{溶解度}{溶解度+100g}$×100%,即饱和溶液中溶解度大则溶质的质量分数大,并结合物质的溶解度随温度变化情况分析解答;
(2)在20℃~30℃之间时硝酸钾和氯化钾具有相同的溶解度,据此解答即可.
解答 解:(1)①P点是t1℃时a与c的溶解度曲线的交点,二者的溶解度相等;
②t2℃时a的溶解度是50g,即100g水中最多溶解50g的a,所以30g a物质加入到50g水中不断搅拌,最多溶解25g,形成75g溶液;
③ab的溶解度随温度升高而增大,c的溶解度随温度升高而减小,所以将t2℃时的a、b、c饱和溶液的温度下降到t1℃时,ab析出晶体,c变为不饱和溶液,溶质的质量分数不变,与降温前相等;饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%,即饱和溶液中溶解度大则溶质的质量分数大,而t1℃时b的溶解度大于a的溶解度大于t2℃时c的溶解度,所以降到t1℃时,三种溶液中溶质的质量分数由大到小的顺序排列是b>a>c;
(2)在20℃~30℃之间时硝酸钾和氯化钾具有相同的溶解度,其取值范围是34.0g<x<37.0g;
故答案为:(1)①当温度为t1℃时,a与c的溶解度相等; ②75 g; ③b>a>c;
(2)34g<x<37g.
点评 本题难度不是很大,主要考查了固体溶解度曲线的意义及根据固体的溶解度曲线来解决相关的问题,从而培养学生分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11. 德国化学家格哈德•艾特尔在固体表面化学的研究中取得了非凡的成就,其成果之一是揭示了氮气与氢气在催化剂表面合成氨的反应过程(如图所示).如图所示微观变化与下列对应叙述正确的是( )
德国化学家格哈德•艾特尔在固体表面化学的研究中取得了非凡的成就,其成果之一是揭示了氮气与氢气在催化剂表面合成氨的反应过程(如图所示).如图所示微观变化与下列对应叙述正确的是( )
 德国化学家格哈德•艾特尔在固体表面化学的研究中取得了非凡的成就,其成果之一是揭示了氮气与氢气在催化剂表面合成氨的反应过程(如图所示).如图所示微观变化与下列对应叙述正确的是( )
德国化学家格哈德•艾特尔在固体表面化学的研究中取得了非凡的成就,其成果之一是揭示了氮气与氢气在催化剂表面合成氨的反应过程(如图所示).如图所示微观变化与下列对应叙述正确的是( )| A. | 原子在化学变化中是可分的 | |
| B. | 符合上述反应过程的顺序是③①② | |
| C. | 此反应有化合物参加 | |
| D. | 对应化合反应方程式为2N+3H2$\stackrel{催化剂}{→}$2NH3 |
9. 全球近140个国家将根据今日签署的《国际防治汞污染公约》在2020年前禁止生产和进出口含汞产品,如:电池,荧光灯,肥皂,化妆品,温度计,血压计等.如图是汞元素的相关信息,其中正确的是( )
全球近140个国家将根据今日签署的《国际防治汞污染公约》在2020年前禁止生产和进出口含汞产品,如:电池,荧光灯,肥皂,化妆品,温度计,血压计等.如图是汞元素的相关信息,其中正确的是( )
 全球近140个国家将根据今日签署的《国际防治汞污染公约》在2020年前禁止生产和进出口含汞产品,如:电池,荧光灯,肥皂,化妆品,温度计,血压计等.如图是汞元素的相关信息,其中正确的是( )
全球近140个国家将根据今日签署的《国际防治汞污染公约》在2020年前禁止生产和进出口含汞产品,如:电池,荧光灯,肥皂,化妆品,温度计,血压计等.如图是汞元素的相关信息,其中正确的是( )| A. | 水银的化学式为Hg | B. | 汞原子的质量为200.6g | ||
| C. | 汞原子的中子数是80 | D. | 汞为非金属元素 |
16.下列变化中,属于物理变化的是( )
| A. |  干冰升华 | B. |  天然气燃烧 | C. |  葡萄酿酒 | D. |  光合作用 |
6.“生活中处处有化学”,下列说法中错误的是( )
| A. | 进到花园能闻到花香,说明分子在不断的运动 | |
| B. | 食用加碘盐,能预防甲状腺肿大疾病 | |
| C. | 打开啤酒瓶盖,啤酒会自动溢出:是因为在温度不变时压强减小,气体溶解度也较小 | |
| D. | 在生铁和钢中,因钢中含碳量高,所以应用广泛:可做炊具和医疗器具 |
10.下列是生活中常见的一些现象,其中属于化学变化的是( )
| A. | 石蜡熔化 | B. | 汽油挥发 | ||
| C. | 洗净的铁锅出现锈渍 | D. | 潮湿的衣服被晒干了 |
11.下列反应属于复分解反应的是( )
| A. |  | B. |  | ||
| C. | 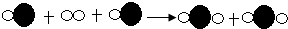 | D. | 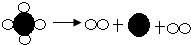 |
 2015年4月6日18时福建漳州古雷化工厂,盛有二甲苯的储油罐漏油着火,附近三个储油罐也相继被引爆炸,7日16时大火被扑灭.17时40分油罐又死灰复燃,再次被扑灭.火场上空黑烟密布,气味呛人.
2015年4月6日18时福建漳州古雷化工厂,盛有二甲苯的储油罐漏油着火,附近三个储油罐也相继被引爆炸,7日16时大火被扑灭.17时40分油罐又死灰复燃,再次被扑灭.火场上空黑烟密布,气味呛人.