题目内容
5.工业上生产电路板及处理废液的工艺流程如图: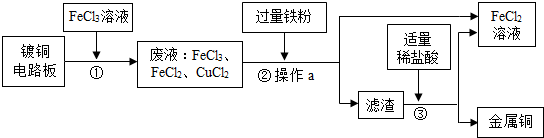
(1)操作a是过滤.
(2)步骤②加入过量铁粉,除能与废液中的FeCl3反应外,还可发生反应的化学方程式为Fe+CuCl2═Cu+FeCl2.
(3)步骤③加入稀盐酸,充分搅拌,当观察到没有气泡冒出现象时,说明滤渣只剩铜.步骤③发生的化学方程式为Fe+2HCl═FeCl2+H2↑.
(4)步骤②③所得FeCl2可与一种单质发生化合反应,生成可循环使用的FeCl3.请写出该反应的化学方程式2FeCl2+Cl2═2FeCl3.
分析 (1)通过操作a得到的滤渣和液体,故是过滤操作;
(2)根据金属活动性顺序可以判断出铁可以将铜置换出来,可以据此写出该反应的化学方程式;
(3)由于加入的铁粉是过量的,所以在加入盐酸时铁要和盐酸反应,可以据此答题;
(4)根据氯化亚铁与氯气的反应作出解答.
解答 解:(1)操作a得到的滤渣和液体,故是过滤操作,故填:过滤;
(2)铁能与氯化铜反应生成氯化亚铁和铜,故填:Fe+CuCl2═Cu+FeCl2;
(3)铁能与盐酸反应生成氢气,而铜不与盐酸反应,故当观察到没有气泡产生,说明剩余的是铜,故填:没有气泡冒出,Fe+2HCl═FeCl2+H2↑;
(4)氯化亚铁与氯气的反应生成氯化铁,故填:2FeCl2+Cl2═2FeCl3.
点评 本题考查的是常见的混合物的分离的知识,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
15.在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表所示:下列推理中正确的是( )
| X | Y | Z | Q | |
| 反应前的质量/g | 20 | 80 | 2 | 21 |
| 反应后的质量/g | 4 | 待测 | 38 | 65 |
| A. | 反应后物质Y的质量为44g | |
| B. | 反应中物质X与Y发生改变的质量之比为1:4 | |
| C. | 反应中Z可能是催化剂 | |
| D. | 若X和Z的相对分子质量分别是16和18,则他们的化学计量数之比是2:1 |
16.一包白色粉末可能有CaCO3、K2SO4、CuSO4、BaCl2、K2CO3的一种或几种,现在进行如下实验.其中说法错误的是( )


| A. | 由操作①可知:白色粉末中一定没有CaCO3、CuSO4 | |
| B. | 由操作②可知:白色粉末中一定没有BaCl2 | |
| C. | 由操作③可知:白色粉末中一定有K2CO3可能有K2SO4 | |
| D. | 滤液b中的溶质有2种 |
13.亚硝酸钠(NaNO2)是一种工业用盐,其水溶液呈碱性.下列说法正确的是( )
| A. | NaNO2溶液能使酚酞溶液变红 | |
| B. | NaNO2溶液不能导电 | |
| C. | NaNO2的相对分子质量为69g | |
| D. | NaNO2中N元素的质量分数为$\frac{14}{23+14+16}$×100% |
17.分类是学习和研究化学的常用方法.下列分类中正确的是( )
| A. | 复合肥料:硝酸钾、碳酸氢铵 | B. | 合金:硬铝、生铁 | ||
| C. | 有机合成材料:涤纶、纯棉布 | D. | 化合物:乙醇、氦气 |
15.下列物质溶于水时,溶液温度明显降低的是( )
| A. | 硝酸铵 | B. | 氯化钠 | C. | 浓硫酸 | D. | 氢氧化钠 |

 (1)用化学用语填空:
(1)用化学用语填空: