题目内容
14.如图为制取气体的常用装置,回答下列问题: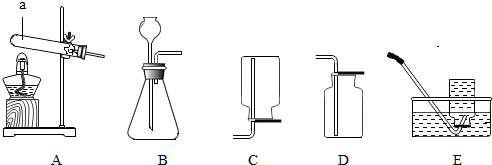
(1)仪器a的名称是试管.
(2)A与D连接可制取氧气,反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)B、C连接时,制得的气体应具有的物理性质是密度比空气小.
分析 (1)根据实验室常用仪器解答;
(2)根据实验室中选择A和D制取和收集氧气,其中A装置需要加热,故可以选择高锰酸钾或氯酸钾与二氧化锰的混合物来制取;
(3)根据C是向下排空法收集解答.
解答 解:
(1)根据实验室常用仪器可知:a是试管;
(2)A装置是在加热的条件下来制取氧气,可以是加热高锰酸钾,也可以是加热氯酸钾与二氧化锰的混合物来制取;试管口无棉花,用加热氯酸钾制氧气,反应的化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(3)C是向下排空法收集,说明气体的密度比空气小.
答案:
(1)试管
(2)2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(3)密度比空气小
点评 熟练掌握实验室中制取气体的发生装置和收集装置的选择依据,并能作出正确的选择,记住常见气体制取的反应原理,并能够正确书写化学方程式.

练习册系列答案
相关题目
2.向饱和澄清的氢氧化钙溶液中加入一定量的CaO,充分反应后恢复到原来温度.下列说法中,正确的是( )
| A. | 溶液中溶质质量增多,溶液的质量减少 | |
| B. | 溶液中溶质质量增多,溶液的质量增加 | |
| C. | 溶液中水的质量减少,溶质质量分数不变 | |
| D. | 溶液中水的质量减少,溶质质量分数增大 |
9.食盐是重要的调味品,在生产生活中的应用非常广泛.
(1)16%的食盐水用于选种,配制200g16%的食盐水,应称取食盐32g.
(2)世界上大部分的金属钠都是通过电解熔融的氯化钠制得的,该过程发生反应的化学方程式
为2NaCl$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑.
(3)亚硝酸钠是一种工业盐,常用于腌肉,和食盐很像,但一次食用3g可使人中毒死亡.下表为亚硝酸钠和食盐的部分性质对比表:
依据表中信息,写出一种鉴别氯化钠和亚硝酸钠的方法取两种固体各37克与烧杯中,分别加入100克20°C水充分搅拌,有固体剩余的是食盐,无固体剩余的是亚硝酸钠..
(1)16%的食盐水用于选种,配制200g16%的食盐水,应称取食盐32g.
(2)世界上大部分的金属钠都是通过电解熔融的氯化钠制得的,该过程发生反应的化学方程式
为2NaCl$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑.
(3)亚硝酸钠是一种工业盐,常用于腌肉,和食盐很像,但一次食用3g可使人中毒死亡.下表为亚硝酸钠和食盐的部分性质对比表:
| 味道 | 溶解度(20°C) | 水溶液pH | 稳定性 | |
| NaCl | 咸味 | 36g | 7 | 801℃熔化 |
| NaNO2 | 咸味 | 67g | 9 | 320℃分解 |
19.妈妈买来一瓶管道通,商品标识如下表:
小明欲测定标识中碳酸钠的含量是否属实,做了以下实验:取10g 管道通样品,加入足量水,待完全冷却后滤去不溶物,向滤液中加入足量的稀盐酸,生成二氧化碳0.88g(假设管道通其他成分不参加化学反应).请通过计算说明碳酸钠的标识是否属实(请写出计算过程).
 | 商品名 | 固体管道疏通剂 |
| 主要成分 | 氢氧化钠60% 碳酸钠15% | |
| 注意事项 | 不要与皮肤接触 | |
| 含量 | 600g |
3.下列图示的实验操作中,正确的是( )
| A. |  | B. |  | C. |  | D. |  |
4.下列材料中属于合成材料的是( )
| A. | 棉麻织物 | B. | 玻璃钢 | C. | 有机玻璃 | D. | 铝合金 |
 我市银滩是国家“AAAA”级滨海旅游度假区,有漫长的海岸线,海洋资源十分丰富,海水中含有大量的化学物质.
我市银滩是国家“AAAA”级滨海旅游度假区,有漫长的海岸线,海洋资源十分丰富,海水中含有大量的化学物质.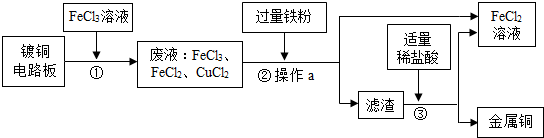
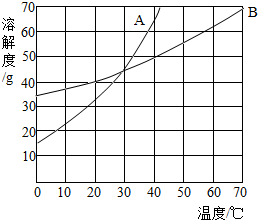 如图是A物质和B物质的溶解度曲线,回答下列问题:
如图是A物质和B物质的溶解度曲线,回答下列问题: