题目内容
10. (1)用化学用语填空:
(1)用化学用语填空:①地壳中含量最多的元素O;
②构成氯化镁的阳离子Mg2+;
③氧化铁中铁元素的化合价$\stackrel{+3}{Fe}$2O3;
④最常用的溶剂H2O.
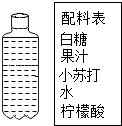
(2)根据图中自制汽水的配料回答问题.
①柠檬酸的pH<7(填“<”、“=”或“>”),
②小苏打的化学式为NaHCO3,属于无机物(填“有机物”或“无机物”).
③配料中富含维生素的是果汁.
分析 (1)元素符号可以表示一种元素,还可以表示该元素的1个原子,有时还可以表示一种物质,例如金属元素的元素符号可以表示该金属元素组成的物质;
构成氯化镁的阳离子是镁离子,每个镁离子带2个单位正电荷;
氧化铁中铁元素的化合价是+3;
最常用的溶剂是水,每个水分子由2个氢原子和1个氧原子构成;
(2)显酸性的溶液的pH小于7;
小苏打是碳酸氢钠的俗称,属于无机物;
水果、蔬菜中富含维生素.
解答 解:(1)①地壳中含量最多的元素是氧元素,可以表示为O;
②构成氯化镁的阳离子是镁离子,可以表示为Mg2+;
③氧化铁中铁元素的化合价是+3,可以表示为$\stackrel{+3}{Fe}$2O3;
④最常用的溶剂是水,可以表示为H2O.
故填:O; Mg2+;$\stackrel{+3}{Fe}$2O3;H2O.
(2)①柠檬酸显酸性,pH<7;
②小苏打的化学式为NaHCO3,碳酸氢钠虽然是含有碳元素的化合物,但是由于性质和无机物相似,因此属于无机物;
③配料中富含维生素的是果汁.
故填:<;NaHCO3;无机物;果汁.
点评 本题主要考查学生对化学用语的书写和理解能力,题目重点考查了学生对化学符号的书写,考查全面,注重基础,题目难度较小.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
20.为了分析某石灰石的纯度,现取8g石灰石放入烧杯中,取40g稀盐酸分四次加入到烧杯中,充分反应剩余固体质量与加入的稀盐酸的量关系如下图所示.(杂质不参加反应).
求:(1)第四次剩余固体物质的质量m=1.6g
(2)该石灰石中碳酸钙的质量分数80%
(3)最终生成二氧化碳的质量是多少g?
| 序号 | 加入的盐酸/g | 剩余固体/g |
| 1 | 10 | 5.5 |
| 2 | 10 | 3 |
| 3 | 10 | 1.6 |
| 4 | 10 | m |
(2)该石灰石中碳酸钙的质量分数80%
(3)最终生成二氧化碳的质量是多少g?
1.如图是某化学反应的微观示意图,其中“○”和“●”表示不同的元素的原子,下列有关说法正确的是( )


| A. | 该反应为置换反应 | |
| B. | 参加反应的“ ”和“ ”和“ ”分子个数比是3:1 ”分子个数比是3:1 | |
| C. | 反应前后分子和原子的总数目不变 | |
| D. | 反应物和生成物中共含有三种元素 |
2.向饱和澄清的氢氧化钙溶液中加入一定量的CaO,充分反应后恢复到原来温度.下列说法中,正确的是( )
| A. | 溶液中溶质质量增多,溶液的质量减少 | |
| B. | 溶液中溶质质量增多,溶液的质量增加 | |
| C. | 溶液中水的质量减少,溶质质量分数不变 | |
| D. | 溶液中水的质量减少,溶质质量分数增大 |
19.妈妈买来一瓶管道通,商品标识如下表:
小明欲测定标识中碳酸钠的含量是否属实,做了以下实验:取10g 管道通样品,加入足量水,待完全冷却后滤去不溶物,向滤液中加入足量的稀盐酸,生成二氧化碳0.88g(假设管道通其他成分不参加化学反应).请通过计算说明碳酸钠的标识是否属实(请写出计算过程).
 | 商品名 | 固体管道疏通剂 |
| 主要成分 | 氢氧化钠60% 碳酸钠15% | |
| 注意事项 | 不要与皮肤接触 | |
| 含量 | 600g |
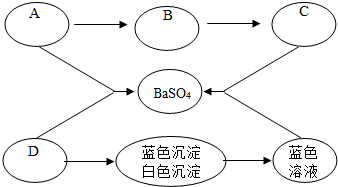
 ”表示两者反应,“→”表示转化成某物质,有些生成物已略去).回答:
”表示两者反应,“→”表示转化成某物质,有些生成物已略去).回答: