题目内容
19.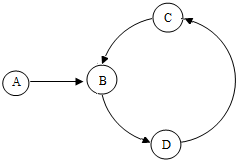 已知A、B、C、D是四种不同类别的物质且含有同一种元素,B在常温下为液体,C为一种难溶性盐,它们的转化关系如图所示.
已知A、B、C、D是四种不同类别的物质且含有同一种元素,B在常温下为液体,C为一种难溶性盐,它们的转化关系如图所示.(1)A物质所属的类别是酸或单质.
(2)B→D的反应是放热(填“吸热”或“放热”)反应.
(3)C→B反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
(4)写出一个符合题意的非基本反应类型的化学方程式Ca(OH)2+CO2═CaCO3↓+H2O.
分析 根据A、B、C、D是四种不同类别的物质且含有同一种元素,B在常温下为液体,C为一种难溶性盐,会产生B,所以B是水,C可以是难溶性的碳酸钙,则D是氢氧化钙,则A可以是单质或酸,然后将推出的物质进行验证即可.
解答 解:A、B、C、D是四种不同类别的物质且含有同一种元素,B在常温下为液体,C为一种难溶性盐,会产生B,所以B是水,C可以是难溶性的碳酸钙,则D是氢氧化钙,则A可以是单质或酸,因此:
(1)根据推导可知A物质所属的类别酸或单质;故填:酸或单质;
(2)B是水,水和氧化钙反应产生氢氧化钙,会放出大量的热;故填:放热;
(3)C→B可以是碳酸钙和盐酸反应产生氯化钙、水和二氧化碳;故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(4)氢氧化钙和二氧化碳反应产生碳酸钙沉淀和水,不属于基本反应类型;故填:Ca(OH)2+CO2═CaCO3↓+H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
9.下列离子能在pH=13的溶液中大量共存的是( )
| A. | SO42-、Cl-、Na+、H+ | B. | K+、SO42-、Cu2+、NO3- | ||
| C. | SO42-、Cl-、K+、Na+、 | D. | Ca2+、CO32-、Na+、Cl- |
7.我们生活在一个多姿多彩的世界,下列有颜色的物质不属于纯净物的是( )
| A. | 赤铁矿 | B. | 红磷 | C. | 高锰酸钾 | D. | 氧化铜 |
11.对如图所示实验的分析错误的是( )
| A. | 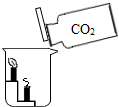 如图中实验说明二氧化碳不能燃烧,也不支持燃烧,且密度比空气大 | |
| B. |  如图中物体在力的作用下做圆周运动,说明物体的运动需要力来维持 | |
| C. |  如图实验说明光在同种均匀介质中沿直线传播 | |
| D. |  如图实验中烧杯内壁有水珠生成,说明甲烷中含有氢元素 |
8. 按如图所示装置进行实验(图中铁架台均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )
按如图所示装置进行实验(图中铁架台均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )
 按如图所示装置进行实验(图中铁架台均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )
按如图所示装置进行实验(图中铁架台均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )| A. | 甲:Na2CO3、稀 HC1;乙:NaOH 溶液 | B. | 甲:Zn,稀 H2SO4;乙:Ba (NO3) 2溶液 | ||
| C. | 甲:MgO,稀盐酸;乙:AgNO3 | D. | 甲:Cu、稀 H2SO4;乙:BaCl2溶液 |
9.某学校化学兴趣小组的同学们在实验室发现一瓶石灰水试剂瓶瓶壁和瓶塞周围有一些白色粉末,为了弄清楚白色粉末的成分及形成原因,他们进行了如下探究:
【提出问题】白色粉末的成分的什么?
【做出猜想】①甲同学认为可能是CaCO3:原因是石灰水与空气中的CO2反应.
②乙同学认为可能是氢氧化钙:原因是溶剂蒸发,石灰水中的溶质结晶析出.
③丙同学认为还可能是碳酸钙和氢氧化钙.
【实验探究】甲同学取白色粉末于试管中,加少量的水、震荡,发现试管底部有白色固体,于是他得出白色粉末是CaCO3的结论.乙同学认为甲同学的结论不严密,理由是氢氧化钙微溶于水,如果白色粉末中含有氢氧化钙,不一定能够完全溶于少量的水.
为了得出较严密的结论,他们进行了下表所示实验,请完成实验报告:
由上述实验可知,白色粉末成分的猜想丙同学是正确的.
【拓展反思】实验室清洗装石灰水试剂瓶内壁上的白色粉末时,可用稀盐酸,请写出其中可能发生的反应的化学方程式(写出一个即可):CaCO3+2HCl═CaCl2+H2O+CO2↑,或Ca(OH)2+2HCl═CaCl2+2H2O.
【提出问题】白色粉末的成分的什么?
【做出猜想】①甲同学认为可能是CaCO3:原因是石灰水与空气中的CO2反应.
②乙同学认为可能是氢氧化钙:原因是溶剂蒸发,石灰水中的溶质结晶析出.
③丙同学认为还可能是碳酸钙和氢氧化钙.
【实验探究】甲同学取白色粉末于试管中,加少量的水、震荡,发现试管底部有白色固体,于是他得出白色粉末是CaCO3的结论.乙同学认为甲同学的结论不严密,理由是氢氧化钙微溶于水,如果白色粉末中含有氢氧化钙,不一定能够完全溶于少量的水.
为了得出较严密的结论,他们进行了下表所示实验,请完成实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取上述试管中的上层溶液,滴加1~2滴无色酚酞试液 | 溶液呈红色 | 白色粉末中含有Ca(OH)2 |
| ②往上述试管残留的白色固体中加入稀盐酸 | 有气泡产生 | 白色粉末中含有碳酸钙 |
【拓展反思】实验室清洗装石灰水试剂瓶内壁上的白色粉末时,可用稀盐酸,请写出其中可能发生的反应的化学方程式(写出一个即可):CaCO3+2HCl═CaCl2+H2O+CO2↑,或Ca(OH)2+2HCl═CaCl2+2H2O.


 初三实验操作考试结了,某班同学清理实验室时,发现如下三个内壁都有白色固体的细口瓶,曾经装过标签标示的溶液.同学们想探究白色固体的成分,设计如下实验.
初三实验操作考试结了,某班同学清理实验室时,发现如下三个内壁都有白色固体的细口瓶,曾经装过标签标示的溶液.同学们想探究白色固体的成分,设计如下实验.