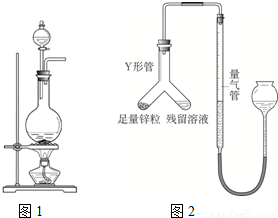
题目内容
实验室常用MnO2+4HCl(浓)?MnCl2+Cl2↑+2H2O的反应来制取氯气(Cl2).当有17.4g二氧化锰完全反应时,能生成多少克的氯气?分析:根据反应的化学方程式MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,由参加反应的17.4g二氧化锰可计算生成氯气的质量.
| ||
解答:解:设生成氯气的质量为x
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
87 71
17.4g x
=
解得x=14.2g
答:能生成14.2克的氯气.
MnO2+4HCl(浓)
| ||
87 71
17.4g x
| 87 |
| 17.4g |
| 71 |
| x |
解得x=14.2g
答:能生成14.2克的氯气.
点评:化根据学方程式表示参加反应的各物质的质量比,由反应中任意一物质的质量可计算反应中其它物质的质量.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
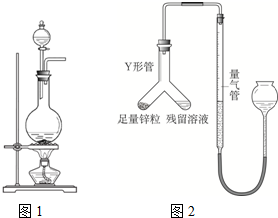 实验室常用MnO2与浓盐酸反应制备Cl2,其反应方程式为:
实验室常用MnO2与浓盐酸反应制备Cl2,其反应方程式为: MnCl2+Cl2↑+2H2O的反应来制取氯气(Cl2)。当有17.4g二氧化锰完全反应时,能生成多少克的氯气?
MnCl2+Cl2↑+2H2O的反应来制取氯气(Cl2)。当有17.4g二氧化锰完全反应时,能生成多少克的氯气? MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O