题目内容
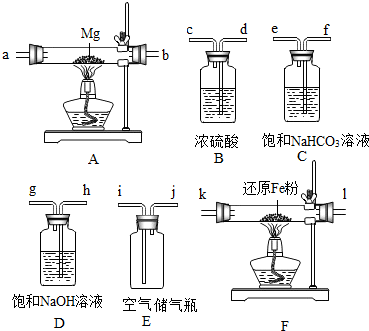
5.某二氧化锰样品中含有杂质炭,为测定该样品中二氧化锰的质量分数,某兴趣小组设计了如下实验方案:在一定量的样品中通入干燥纯净的氧气,使杂质炭在加热条件下反应生成CO2来进行分析测定.
(1)仪器①的名称是长颈漏斗.如果该实验选择图(一)装置来制取氧气,则所反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.其中二氧化锰的起到催化作用.
(2)用图(二)装置可收集和干燥氧气:若烧瓶充满水来收集氧气,气体应从a(“a”或“b”)端通入.
(3)图(三)是用干燥纯净的O2与样品反应来测定二氧化锰质量分数的装置,装置③中装有碱石灰,其作用是防止空气中的二氧化碳进入氢氧化钠溶液中.
(4)为验证图(三)中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图(四)装置中加入的试剂为B(填字母).
A.NaOH溶液 B.澄清石灰水 C.浓硫酸.
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(2)氧气不易溶于水;
(3)碱石灰能够吸收水蒸气和二氧化碳;
(4)二氧化碳能使澄清石灰水变浑浊.
解答 解:(1)仪器①的名称是长颈漏斗,通过长颈漏斗可以向反应容器中注入液体药品;
如果该实验选择图(一)装置来制取氧气,应该是利用过氧化氢和二氧化锰制取氧气,则反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,其中二氧化锰的起到催化作用.
故填:长颈漏斗;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;催化.
(2)若烧瓶充满水来收集氧气,气体应从a端通入.
故填:a.
(3)装置③中装有碱石灰,其作用是防止空气中的二氧化碳进入氢氧化钠溶液中,以免影响对实验结果的测定.
故填:防止空气中的二氧化碳进入氢氧化钠溶液中.
(4)为验证图(三)中装置②已将CO2吸收完全,可在装置②与③之间加入图(四)装置进行证明,则图(四)装置中加入的试剂为澄清石灰水,如果澄清石灰水不变浑浊,说明装置②已将CO2吸收完全.
故填:B.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.如图反映了钛在元素周期表中的某些信息.下列有关钛的说法不正确的是( )


| A. | 钛属于非金属元素 | B. | 钛的原子序数为22 | ||
| C. | 钛原子的相对原子质量为47.87 | D. | 钛原子核内质子数为22 |
14.下列微粒的结构示意图中表示阳离子的是( )
| A. |  | B. |  | C. |  | D. |  |
20. 如图,某同学用燃烧红磷的方法测定空气中氧气的体积分数,实验后发现测得的氧气体积分数小于$\frac{1}{5}$,对此,你认为下列做法或想法不可取的是( )
如图,某同学用燃烧红磷的方法测定空气中氧气的体积分数,实验后发现测得的氧气体积分数小于$\frac{1}{5}$,对此,你认为下列做法或想法不可取的是( )
 如图,某同学用燃烧红磷的方法测定空气中氧气的体积分数,实验后发现测得的氧气体积分数小于$\frac{1}{5}$,对此,你认为下列做法或想法不可取的是( )
如图,某同学用燃烧红磷的方法测定空气中氧气的体积分数,实验后发现测得的氧气体积分数小于$\frac{1}{5}$,对此,你认为下列做法或想法不可取的是( )| A. | 检查实验装置是否漏气 | |
| B. | 可能红磷的量不足,没有除尽氧气 | |
| C. | 将红磷改成足量的木炭,重新实验 | |
| D. | 没有冷却至室温就打开止水夹,进入瓶内的水减少 |
 2010年10月31日,中国2010年上海世博会闭幕.温家宝总理在回顾盛会给人们留下的经验和启示时称,世博会鲜明弘扬了绿色、环保、低碳等发展新理念,有力证明了科技革命是推动社会进步的强大动力.
2010年10月31日,中国2010年上海世博会闭幕.温家宝总理在回顾盛会给人们留下的经验和启示时称,世博会鲜明弘扬了绿色、环保、低碳等发展新理念,有力证明了科技革命是推动社会进步的强大动力.

