题目内容
10.某同学将4.8g镁条加入到100g的稀硫酸中,恰好完全反应,试计算:(1)该反应生成H2的质量;
(2)这种稀H2SO4溶液的溶质的质量分数;
(3)反应后所得溶液中溶质的质量分数(计算结果保留两位小数).
分析 镁与稀硫酸反应生成硫酸镁和氢气;根据质量守恒定律,根据参加反应的镁的质量,由反应的化学方程式列式计算出生成氢气的质量、稀硫酸的溶质、生成的硫酸锌的质量,进而计算出溶质的质量分数.
解答 解:设生成氢气的质量为x,参加反应的硫酸的质量为y,生成的硫酸镁的质量为z,
Mg+H2SO4═MgSO4+H2↑
24 98 120 2
4.8g y z x
则(1)$\frac{24}{2}=\frac{4.8g}{x}$,解得x=0.4g
(2)$\frac{24}{98}=\frac{4.8g}{y}$,解得y=19.6g,故稀硫酸的溶质质量分数为$\frac{19.6g}{100g}$×100%=19.6%.
(3)$\frac{24}{120}=\frac{4.8g}{z}$,解得z=24g,故反应后测得溶液溶质的质量分数为$\frac{24g}{4.8g+100g-0.4g}×$100%≈22.99%.
故答案为:
(1)0.4克 (2)19.6% (3)22.99%
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
8.下列关于空气的说法中错误的是( )
| A. | 空气中的二氧化碳是参与植物光合作用的重要气体 | |
| B. | 空气中的氮气常用来保存食品 | |
| C. | 空气中的稀有气体通电会发出有颜色的光 | |
| D. | 空气能自净,无需防治污染 |
15.将铁片分别放入下列溶液中充分反应,反应后溶液质量减轻的是( )
(可能用到的相对原子质量:Fe-56 Cu-64 Zn-65 Ag一l08)
(可能用到的相对原子质量:Fe-56 Cu-64 Zn-65 Ag一l08)
| A. | ZnSO4 | B. | FeSO4 | C. | HCl | D. | AgNO3 |
2.有关二氧化碳的实验中,能达到实验目的是( )
| A. | 将燃着的木条伸入集气瓶中,检验二氧化碳是否集满 | |
| B. | 因为二氧化碳在水中的逸出速率大于溶解速率,故也可用排水法收集 | |
| C. | 将二氧化碳气体通入紫色石蕊试液中,证明二氧化碳溶于水显酸性 | |
| D. | 将二氧化碳气体通入CaCl2溶液中,可以看到白色沉淀生成 |
 如图是已破损的维生素C(简写Vc)说明书部分信息.已知维生素C由碳、氢、氧三种元素组成.请回答:
如图是已破损的维生素C(简写Vc)说明书部分信息.已知维生素C由碳、氢、氧三种元素组成.请回答: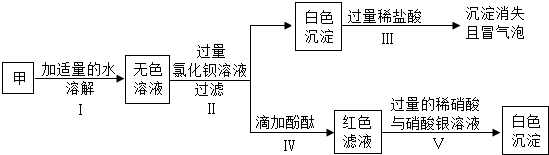

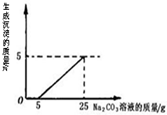 实验室废液桶中收集到大量含有盐酸与氯化钙的废液(不考虑其他杂质).同学们测定该废液中含氯化钙的质量分数,他们取100g废液向其中慢慢滴加质量分数为26.5%的Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如右图所示.
实验室废液桶中收集到大量含有盐酸与氯化钙的废液(不考虑其他杂质).同学们测定该废液中含氯化钙的质量分数,他们取100g废液向其中慢慢滴加质量分数为26.5%的Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如右图所示. 如图表示一瓶氯化锌溶液,该溶液由5g固体放入45g水中配制而成.
如图表示一瓶氯化锌溶液,该溶液由5g固体放入45g水中配制而成.