题目内容
16.中和一定质量的稀硫酸,需要M克NaOH,若改用M克KOH,则反应后溶液的pH为( )| A. | =7 | B. | >7 | C. | <7 | D. | 无法确定 |
分析 根据氢氧化钠、氢氧化钾与硫酸反应的化学方程式,判断改用20克氢氧化钾反应后剩余的是哪一种溶液,再根据当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性;进行分析解答.
解答 解:氢氧化钠、氢氧化钾与硫酸反应的化学方程式分别是:
2NaOH+H2SO4═Na2SO4+2H2O
80 98
2KOH+H2SO4═K2SO4+2H2O
112 98
可知,80份质量的氢氧化钠与98份质量的硫酸恰好完全反应,而98份质量的硫酸能与112份质量的氢氧化钾恰好完全反应;中和一定质量的稀硫酸,需要M克NaOH,则改用M克KOH后,稀硫酸有剩余,溶液显酸性,反应后溶液的pH应当是小于7.
故选:C.
点评 本题难度不大,掌握中和反应应用,根据化学方程式的计算判断出反应后剩余的物质是正确解答本题的关键.

练习册系列答案
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目
7.有关科研机构预测今年的冬季将比往年冷.我国北方某些城市曾用食盐融雪,造成土壤中含盐浓度偏高,使路旁树木死亡.目前专家已研制出一种新型融雪剂,既能融化冰雪,又能起施肥美化树木的作用.具有上述作用的新型融雪剂是( )
| A. | 氯化钠、氯化钙 | B. | 氯化钠、氯化镁 | ||
| C. | 氯化钠、碳酸镁 | D. | 尿素、硝酸钙、硝酸镁 |
11.下列物质放在敞口中一段时间后,质量明显减少的是( )
| A. | 浓硫酸 | B. | 氢氧化钠 | C. | 浓盐酸 | D. | 氯化钠 |
1.为了除去碳酸钙固体(难溶于水)中的碳酸钠杂质(能溶于水),下面操作方法正确的是( )
| A. | 直接过滤 | B. | 溶解后过滤 | C. | 溶解后蒸馏 | D. | 直接蒸馏 |
8.“温室效应”主要是由于下面哪一种气体的含量不断增加造成的( )
| A. | 二氧化硫 | B. | 氧气 | C. | 一氧化碳 | D. | 二氧化碳 |
5.加碘盐中的碘酸钾(KIO3)属于( )
| A. | 氧化物 | B. | 酸 | C. | 碱 | D. | 盐 |
6.氢气还原氧化铜实验得到的固体粉末为氧化铜和铜的混合物,科学兴趣小组的同学对该粉末中单质铜的含量进行测定.三组同学各取10克粉末样品置于烧杯中,然后加入不同质量的同浓度的稀硫酸,充分反应后,对烧杯中剩余固体进行称量.实验数据记录如下:
(1)分析表中数据可知,第2组实验中的剩余固体是铜或者Cu.(写出物质名称或符号)
(2)样品中单质铜的质量分数为80%.
(3)第1组实验中反应了的氧化铜是1.6克,加入的稀硫酸溶质质量分数是多少?(写出计算过程CuO+H2SO4=CuSO4+H2O)
| 组别编号 | 样品质量(克) | 加入稀硫酸质量(克) | 剩余固体质量(克) |
| 1 | 10 | 20 | 8.4 |
| 2 | 10 | 30 | 8 |
| 3 | 10 | 40 | 8 |
(2)样品中单质铜的质量分数为80%.
(3)第1组实验中反应了的氧化铜是1.6克,加入的稀硫酸溶质质量分数是多少?(写出计算过程CuO+H2SO4=CuSO4+H2O)
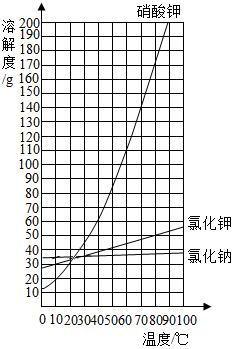 以下是某化学兴趣小组实施的从硝酸钾、氯化钠、氯化钾的混合物(其中氯化钠和氯化钾的质量和小于总质量的3%)中分离出硝酸钾的实验步骤:(三种物质的溶解度曲线见图)
以下是某化学兴趣小组实施的从硝酸钾、氯化钠、氯化钾的混合物(其中氯化钠和氯化钾的质量和小于总质量的3%)中分离出硝酸钾的实验步骤:(三种物质的溶解度曲线见图)