题目内容
20.普通黄铜仅由铜和锌组成,广泛用于制造板材、管材等,也用于铸造机械零件.为测定黄铜中铜的质量分数,取样品10g,分四次向其中加入稀硫酸使之充分反应,实验数据记录如下表:| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀硫酸的质量/g | 10 | 10 | 10 | 10 |
| 剩余固体的质量/g | 8.7 | 7.4 | 7 | 7 |
(1)该过程中发生反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑.
(2)黄铜中铜的质量分数为70%.
(3)画出所加稀硫酸和固体的质量关系图(表示出相对关系即可).
分析 (1)根据金属活动性顺序来分析;
(2)由于锌能与稀硫酸反应而铜不与稀硫酸反应,因此当稀硫酸过量时所剩余固体全部为铜;根据实验记录数据可知,第四次所加入的稀硫酸并未发生发生,此时剩余固体为铜;据此可计算黄铜中铜的质量分数;
(3)根据表格中的数据来分析画出关系图.
解答 解:(1)在金属活动顺序中,锌排在氢的前面,铜排在氢的后面,所以锌能与稀硫酸反应生成硫酸锌和氢气,铜与稀硫酸不反应,故填:Zn+H2SO4=ZnSO4+H2↑;
(2)锌能和稀硫酸反应,而铜不能和稀硫酸反应,加入稀硫酸完全反应后,剩余固体为铜,则铜的质量是7g,黄铜中铜的质量分数为:$\frac{7g}{10g}×100%$=70%;故填:70%;
(3)横坐标表示加入稀硫酸的质量,纵坐标表示固体质量,由表格数据可知,每加入10g稀硫酸能反应1.3g锌,则第3次反应掉0.4g锌,需要稀硫酸的质量为x,则
$\frac{1.3g}{10g}=\frac{0.4g}{x}$
x≈3.1g
则图象的转折点为(23.1,7)
故为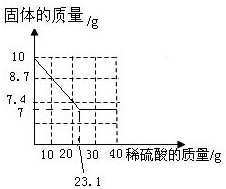 .
.
点评 本题考查识图和根据化学方程式进行计算方面的知识,第三次加入稀硫酸后,剩余固体的质量是7g,比第二次减少0.4g,小于1.3g,说明锌已经完全反应.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
10.某反应的微观示意图如下,其中不同的圆球代表不同的原子,有关说法正确的是( )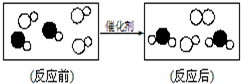

| A. | 化学反应前后分子的种类一定不变 | |
| B. | 原子在化学变化中的数目、种类都不变 | |
| C. | 图中的生成物全部是化合物 | |
| D. | 参加反应的两种分子的个数比为2:3 |
11.下列物质的用途与其化学性质相关的是( )
| A. | 氮气用于磁悬浮列车 | B. | 铜丝用作导线 | ||
| C. | 氧气用于医疗急救 | D. | 稀有气体制成霓虹灯 |
8.化学实验过程中要规范操作,注意实验安全.下列做法错误的是( )
| A. | 用蒸发皿蒸发浓缩液体时要用玻璃棒搅拌 | |
| B. | 给试管中的药品加热时试管口一定要略向下倾斜 | |
| C. | 点燃氢气前,一定要先检验氢气的纯度 | |
| D. | 用高锰酸钾制取并用排水法收集氧气完毕,先从水中移出导管,再熄灭酒精灯 |
15.地壳中含量最多的非金属元素、金属元素、空气中含量最多的元素组成的物质( )
| A. | Al3O2 | B. | SiO2 | C. | Al(NO3)3 | D. | Fe(NO3)3 |
14.下列关于化肥和农药的说法错误的是( )
| A. | 硝酸钾是一种复合肥 | |
| B. | 化肥对提高农作物产量有重要作用 | |
| C. | 农药本身有毒,应该禁止施用 | |
| D. | 目前施用农药仍是最重要的作物保护手段 |




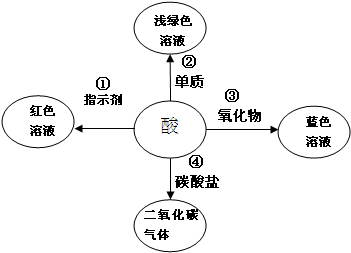 酸是很重要的物质,在初三化学学习中,很多化学实验都用到酸(盐酸和硫酸).酸能够跟很多种类的物质发生化学反应,如图是对酸的部分化学性质的归纳.
酸是很重要的物质,在初三化学学习中,很多化学实验都用到酸(盐酸和硫酸).酸能够跟很多种类的物质发生化学反应,如图是对酸的部分化学性质的归纳.