题目内容
8.下列实验现象描述错误的是( )| A. | 打开浓盐酸的瓶盖,瓶口出现白烟 | |
| B. | 镁带在空气中燃烧发出耀眼的白光 | |
| C. | 硫粉在氧气中燃烧,发出蓝紫色火焰 | |
| D. | 电解水时正极产生的气体体积比负极产生的气体体积少 |
分析 A、根据浓盐酸的挥发性解答;
B、根据镁带燃烧的现象解答;
C、根据硫粉在氧气中燃烧的现象解答;
D、根据电解水时正氧负氢、氢二氧一解答.
解答 解:A、打开浓盐酸的瓶盖,瓶口出现白雾,错误;
B、镁带在空气中燃烧发出耀眼的白光,正确;
C、硫粉在氧气中燃烧,发出蓝紫色火焰,正确;
D、电解水时正极产生的气体体积比负极产生的气体体积少,正确;
故选A.
点评 本题考查的是对常见的实验现象的描述,完成此题,可以依据已有的实验现象进行,要注意白烟和白雾的区别.

练习册系列答案
 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
18.关于学习化学,以下说法错误的是( )
| A. | 化学是一门以实验为基础的学科 | B. | 学习化学可以随意尝化学药品 | ||
| C. | 化学可以帮助人们开发新资源 | D. | 化学可以帮助人们研制新材料 |
3.掌握化学用语是学好化学的重要基础之一.下列化学用语与对应含义相符的是( )
| A. | H2O2--过氧化氢 | B. | 2H--2个氢分子 | C. | O2--2个氧原子 | D. | $\stackrel{+1}{Na}$--钠离子 |
17.取70g某温度下的硝酸钾饱和溶液,将其恒温蒸发10g水,析出4g硝酸钾固体,则剩余溶液中所含溶质质量为( )
| A. | 16 g | B. | 20 g | C. | 40 g | D. | 56 g |
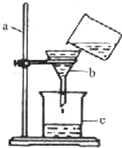 有一种含有碎菜叶、碎塑料薄膜、泥沙,还具有一定臭味的生活污水(生活污水的成分很复杂,此处已作简化),将其经除渣去臭处理后可转化为厕所的清洗用水.
有一种含有碎菜叶、碎塑料薄膜、泥沙,还具有一定臭味的生活污水(生活污水的成分很复杂,此处已作简化),将其经除渣去臭处理后可转化为厕所的清洗用水.
 在2014年南宁市理化实验操作考试中.小刚同学选择了稀盐酸、氢氧化钠溶液、酚酞溶液三种试剂,按如图所示进行酸碱中和反应的实验.请回答:
在2014年南宁市理化实验操作考试中.小刚同学选择了稀盐酸、氢氧化钠溶液、酚酞溶液三种试剂,按如图所示进行酸碱中和反应的实验.请回答: ”、“
”、“ ”表示不同元素的原子,则下列图示表示的气体物质中,属于单质的是B,属于化合物的是A,属于混合物的是C(请用序号填空)
”表示不同元素的原子,则下列图示表示的气体物质中,属于单质的是B,属于化合物的是A,属于混合物的是C(请用序号填空)