题目内容
9.水是生命之源,请回答下列有关水的化学知识:(1)自来水生产中,常用活性炭除去水中的异味;
(2)水变成水蒸气过程中,不发生变化的是AB(填字母序号);
A.分子质量 B.分子种类 C.分子间隔
(3)通过电解水以及氢气燃烧的实验,均可以证明水是由氢、氧元素组成的;通电分解水时,正、负极生成的气体质量比是8:1..
分析 (1)根据活性炭具有吸附性解答;
(2)根据水变成水蒸气的过程属于物理变化解答;
(3)根据电解水实验的现象和结论分析.
解答 解:
(1)活性炭具有吸附性,净水时加入活性炭的目的吸附水中的色素和异味;
(2)水变成水蒸气的过程中,不发生变化的是分子质量和分子种类,分子间隔变大.
故填:AB.
(3)通过电解水以及氢气燃烧的实验,均可以证明水是由氢、氧元素组成的;通电分解水时,正、负极生成的气体体积比是1:2,质量比是8:1.
答案:
(1)活性炭;
(2)AB;
(3)氢气燃烧;8:1.
点评 电解水生成氢气和氧气,说明水是由氢元素和氧元素组成的,同时说明在化学变化中,分子可分,原子不可分.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.装运化学药品氢氧化钠的车辆应贴的图标是( )
| A. |  | B. |  | C. |  | D. |  |
20.“对比实验”是化学学习中行之有效的思维方法,以下实验没有体现“对比”的是( )
| A. | 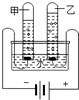 探究水的组成 | B. | 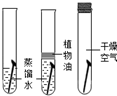 探究铁钉锈蚀的条件 | ||
| C. | 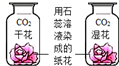 探究CO2的性质 | D. | 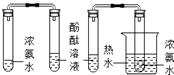 探究分子运动速率与温度关系 |
17.根据所学知识填空:
(1)化学中常用下列词语描述物质的性质:A.可燃性B.吸水性C.溶解性D.还原性.请用序号填空:
①浓硫酸常用作干燥剂是因为它具有B.②氢气作为燃料是因为它具有A.
③焦炭用来冶炼金属D.④能否用排水法收集气体是根据气体的C.
(2)如图是超市里一种盐汽水的营养成分表.
营养成分表
①该汽水中能量主要由碳水化合物提供.该汽水中含人体每天所需的六大营养素有3种.
②“钠115毫克”是指元素(填“单质”或“元素”)的质量.
③小虎同学欲探究该盐汽水的酸碱性,取少量汽水于试管中,滴加紫色石蕊试液,石蕊试液变红色,则该汽水显酸性,经查阅资料该汽水中溶有大量的CO2,要提高100mL水中CO2的溶解量,可加压、降温(写两种方法即可).
(1)化学中常用下列词语描述物质的性质:A.可燃性B.吸水性C.溶解性D.还原性.请用序号填空:
①浓硫酸常用作干燥剂是因为它具有B.②氢气作为燃料是因为它具有A.
③焦炭用来冶炼金属D.④能否用排水法收集气体是根据气体的C.
(2)如图是超市里一种盐汽水的营养成分表.
营养成分表
| 项目 | 每100毫升 | 单位 | 营养素参考值% |
| 能量 | 43 | 千焦 | 1% |
| 蛋白质 | 0 | 克 | 0% |
| 脂肪 | 0 | 克 | 0% |
| 碳水化合物 | 25 | 克 | 1% |
| 钠 | 115 | 毫克 | 6% |
②“钠115毫克”是指元素(填“单质”或“元素”)的质量.
③小虎同学欲探究该盐汽水的酸碱性,取少量汽水于试管中,滴加紫色石蕊试液,石蕊试液变红色,则该汽水显酸性,经查阅资料该汽水中溶有大量的CO2,要提高100mL水中CO2的溶解量,可加压、降温(写两种方法即可).
4.只用一种试剂鉴别NaOH、HCl、NaCl三种无色溶液,这种试剂是( )
| A. | 紫色石蕊试液 | B. | 酚酞试液 | C. | AgNO3溶液 | D. | BaCl2溶液 |
14.对于下列5种化学符号:①H;②Fe2+;③Cu;④SO2;⑤NaCl.有关说法正确的是( )
| A. | ①只能表示氢元素 | |
| B. | ③只能表示铜原子 | |
| C. | ③④⑤能表示物质的化学式 | |
| D. | ②中的“2”表示铁离子带2个单位正电荷 |
1.下列物质的用途正确的是( )
| A. |  氧气用于炼钢 | B. |  聚氯乙烯用于食物包装 | ||
| C. |  二氧化碳气体用于人工降雨 | D. |  氮气用于霓虹灯 |
18.草木灰是农家肥料,主要含钾盐.请回答相关问题.
【分离提纯】
Ⅰ.在烧杯里放一定量的草木灰,加入水,同时用玻璃棒搅拌.
Ⅱ.把烧杯中的草木灰连同浸出液一起过滤.
Ⅲ.把滤液倒入蒸发皿里,加热,用玻璃棒搅拌.当蒸发到大量固体析出_时,停止加热.
【定性分析】取分离提纯所得的晶体进行实验.
【实验反思】
(1)实验一中发生反应的化学方程式有K2CO3+2HCl=2KCl+H2O+CO2↑,CO2+Ca(OH)2=CaCO3↓+H2O.
(2)为证明实验二中的溶液呈碱性是由CO32-引起的,再向红色溶液中加入过量的氯化钙溶液,当看到红色逐渐消失,且溶液中产生白色沉淀时即可证明.
(3)草木灰不能与下列化肥中的C(填“序号”)混合使用.
A.CO(NH2)2 B.KNO3 C.NH4Cl D.磷矿粉
【定量分析】测定草木灰中碳酸钾的含量(假设草木灰中的杂质不含碳酸根,不与酸反应)
测定原理:利用图一中的A装置将草木灰中的碳酸钾转化成二氧化碳,通过测定二氧化碳的质量或体积,计算出草木灰中的碳酸钾的质量.
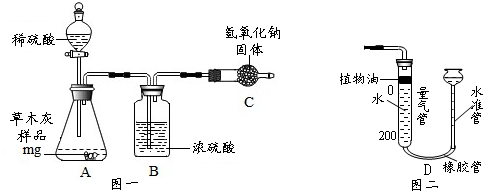
(4)实验前,向图一A的分液漏斗中加入水,用弹簧夹夹住A、B间的橡胶管….这样做的目的是检查装置的气密性;装置B的作用是吸水.
(5)图一装置中欲测定生成的二氧化碳的质量,需测定的数据是C在反应前后的质量.
(6)图二中的D装置可用于测定生成的二氧化碳的体积,测定时不需要(“需要”、“不需要”)等A、B装置中的空气排尽时再连接.
(7)用图一测出的碳酸钾的质量分数偏小,可能的原因是产生的二氧化碳未完全被C吸收.
【分离提纯】
Ⅰ.在烧杯里放一定量的草木灰,加入水,同时用玻璃棒搅拌.
Ⅱ.把烧杯中的草木灰连同浸出液一起过滤.
Ⅲ.把滤液倒入蒸发皿里,加热,用玻璃棒搅拌.当蒸发到大量固体析出_时,停止加热.
【定性分析】取分离提纯所得的晶体进行实验.
| 实验序号 | 实验操作 | 实验现象 | 实验结论 |
| 实验一 | 取样,加入足量的稀盐酸,将生成的气体通入澄清的石灰水 | 石灰水变浑浊 | 该晶体中含有碳酸根离子 |
| 实验二 | 取样,溶于水滴入酚酞 | 溶液变红色 | 溶液呈碱性 |
(1)实验一中发生反应的化学方程式有K2CO3+2HCl=2KCl+H2O+CO2↑,CO2+Ca(OH)2=CaCO3↓+H2O.
(2)为证明实验二中的溶液呈碱性是由CO32-引起的,再向红色溶液中加入过量的氯化钙溶液,当看到红色逐渐消失,且溶液中产生白色沉淀时即可证明.
(3)草木灰不能与下列化肥中的C(填“序号”)混合使用.
A.CO(NH2)2 B.KNO3 C.NH4Cl D.磷矿粉
【定量分析】测定草木灰中碳酸钾的含量(假设草木灰中的杂质不含碳酸根,不与酸反应)
测定原理:利用图一中的A装置将草木灰中的碳酸钾转化成二氧化碳,通过测定二氧化碳的质量或体积,计算出草木灰中的碳酸钾的质量.

(4)实验前,向图一A的分液漏斗中加入水,用弹簧夹夹住A、B间的橡胶管….这样做的目的是检查装置的气密性;装置B的作用是吸水.
(5)图一装置中欲测定生成的二氧化碳的质量,需测定的数据是C在反应前后的质量.
(6)图二中的D装置可用于测定生成的二氧化碳的体积,测定时不需要(“需要”、“不需要”)等A、B装置中的空气排尽时再连接.
(7)用图一测出的碳酸钾的质量分数偏小,可能的原因是产生的二氧化碳未完全被C吸收.
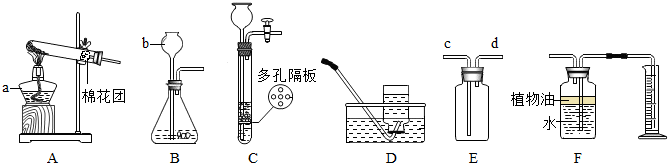 (1)写出下列仪器名称:a酒精灯;b长颈漏斗.
(1)写出下列仪器名称:a酒精灯;b长颈漏斗.