题目内容
20.某无色气体,可能含有H2、CO、CO2、H2O中的一种或多种,现将该气体依次经过下列装置处理(假设每步作用均完全).有关的实验现象是:Ⅰ、A装置质量增重;Ⅱ、B装置中的固体由黑变红;Ⅲ、C装置中无水硫酸铜变蓝;Ⅳ、D装置质量增加.请回答下列问题.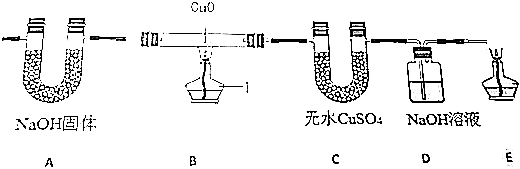
①装置C中无水硫酸铜变蓝的原因是CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O(用化学方程式表示),装置C的作用是吸收气体中的水蒸气;
②由现象Ⅱ和Ⅳ可知该混合气体中肯定含有CO,该物质在装置B中与CuO反应的化学方程式是CuO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
③有同学认为上图方案不合理,请你指出存在的问题未反应完的一氧化碳气通过D后会携带水蒸气,对后面的用酒精灯点燃会产生影响,改进方案是在装置D、E之间增加一个干燥装置.
分析 ①根据无水硫酸铜遇水变蓝的性质进行分析;
②根据氢气和一氧化碳具有还原性,二氧化碳会与氢氧化钠反应进行分析;
③根据通过D后气体可能会携带水蒸气进行分析.
解答 解:①根据C装置中无水硫酸铜变蓝知,B装置中的反应有水生成,而无色气体中可能含有H2、CO、CO2、H2O中的一种或多种,可判知是氢气与氧化铜在加热条件下反应生成了水,该反应用化学方程式表示为:CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,装置C的作用是吸收气体中的水蒸气;
②根据D装置质量增加可判断B装置中的反应有二氧化碳生成,一氧化碳具有还原性,在加热条件下可与B装置中的氧化铜反应使固体由黑变红同时生成二氧化碳气体,于是由现象Ⅱ和Ⅳ可判断该混合气体中肯定含有CO,CO在装置B中与CuO反应的化学方程式是:CuO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
③未反应完的一氧化碳气通过D后会携带水蒸气,对后面的用酒精灯点燃会产生影响,只要在点燃之前将水蒸气除去就可以了,故在装置D、E之间增加一个干燥装置即可.
故答案为:①CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;吸收气体中的水蒸气;
②CO; CuO+CO $\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2;
③未反应完的一氧化碳气通过D后会携带水蒸气,对后面的用酒精灯点燃会产生影响;在装置D、E之间增加一个干燥装置即可.
点评 本题考查了氢气、一氧化碳还原氧化铜,二氧化碳与碱反应以及混合物分离除杂.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
1.加油站、面粉加工厂、煤矿矿井内、纺织厂必贴的图标是( )
| A. |  | B. |  | C. |  | D. |  |




