题目内容
3.今有四种粒子的结构示意图,下列说法不正确的是( )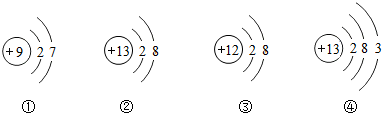
| A. | 它们表示三种元素 | |
| B. | ④表示的元素核内质子数为13 | |
| C. | ②③都表示阳离子 | |
| D. | ①表示的粒子在化学反应中易失去电子 |
分析 A、根据不同种元素最本质的区别是质子数不同,进行分析判断.
B、根据结构示意图的意义解答.
C、当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子.
D、若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子.
解答 解:A、不同种元素最本质的区别是质子数不同,②和④核内质子数相同,属于同一种元素,图中共表示3种元素,故选项说法正确.
B、由④结构示意图可知:④表示的核内质子数为13,故选项说法正确.
C、②③均质子数>核外电子数,均为阳离子,故选项说法正确.
D、①表示的粒子最外层电子数是7,大于4,在化学反应中易得到1个电子而形成阴离子,故选项说法错误.
故选:D.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系等是解题的关键.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
14.防火、灭火、自救等安全知识是每个人应该了解的生活常识.下列做法错误的是( )
| A. | 发现家中燃气泄露,及时打开排气扇 | |
| B. | 炒菜时油锅着火用锅盖盖灭 | |
| C. | 乘坐公共交通工具时严禁携带易爆品 | |
| D. | 火场逃生时在有烟雾的地方捂住口鼻匍匐前进 |
11.如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是( )
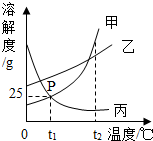

| A. | P点表示甲、丙两种物质的饱和溶液质量相等 | |
| B. | t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液 | |
| C. | t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1:4 | |
| D. | 将三种物质的溶液从t2℃降至t1℃,溶质质量分数最小的一定是丙物质 |
18.实验探究一:课本第二单元课后作业中有“寻找新的催化剂”的探究内容,实验中学探究小组据此设计了如下探究方案.
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
【拓展应用】
己知CuSO4也可作为过氧化氢分解的催化剂.向101.2g一定溶质质量分数的过氧化氢溶液中加入2g CuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气3.2g.
实验探究二:实验室中的试剂一般要密封保存,否则可能会与空气接触而变质.淅河中学化学学习小组发现一瓶未密封的氢氧化钾固体,对其是否变质进行探究.
【提出猜想】1.未变质 2.部分变质 3.完全变质
【查阅资料】KOH与NaOH性质类似,也能与CO2反应而变质.写出KOH变质的化学方程式为2KOH+CO2═K2CO3+H2O.
【设计实验】
(l)取少量样品于试管中配成溶液,滴加足量稀盐酸有气泡产生,则猜想1不成立.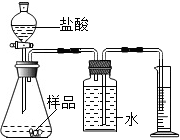
(2)准确称取一定质量的固体样品,放在如图所示装置中进行实验,根据CO2的体积和密度计算变质产物的质量,从而确定变质情况,你认为这个方案是否可行,并说明理由不可行,因为二氧化碳能够溶于水,并且能和水反应生成碳酸.
(3)请你另外设计一个方案,进一步探究变质情况
【提出问题】红砖粉末能否作为过氧化氢溶液分解的催化剂?如果能,效果如何?
【实验探究】
| 实验步骤 | 实验现象 | 实验结论及解释 |
Ⅰ.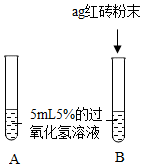 | A中无明显现象,B中产生大量能使带火星木条复燃的气体 | ①产生的气体是氧气 ②红砖粉末能改变过氧化氢分解速率 |
| Ⅱ.向B试管中重新加入5%的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣 | ①又产生大量能使带火星木条复燃的气体 ②滤渣质量等于ag | 红砖粉末的质量和化学性质在反应前后均没有发生变化,能作过氧化氢分解的催化剂 |
Ⅲ.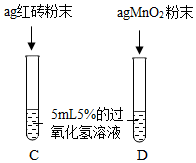 | 两试管中均产生气泡且加入二氧化锰的试管中产生气泡的速率比加入红砖粉末的快 | 红砖粉末的催化效果没有二氧化锰粉末好 |
己知CuSO4也可作为过氧化氢分解的催化剂.向101.2g一定溶质质量分数的过氧化氢溶液中加入2g CuSO4粉末,充分反应后得到溶质质量分数为2%的溶液,则生成氧气3.2g.
实验探究二:实验室中的试剂一般要密封保存,否则可能会与空气接触而变质.淅河中学化学学习小组发现一瓶未密封的氢氧化钾固体,对其是否变质进行探究.
【提出猜想】1.未变质 2.部分变质 3.完全变质
【查阅资料】KOH与NaOH性质类似,也能与CO2反应而变质.写出KOH变质的化学方程式为2KOH+CO2═K2CO3+H2O.
【设计实验】
(l)取少量样品于试管中配成溶液,滴加足量稀盐酸有气泡产生,则猜想1不成立.

(2)准确称取一定质量的固体样品,放在如图所示装置中进行实验,根据CO2的体积和密度计算变质产物的质量,从而确定变质情况,你认为这个方案是否可行,并说明理由不可行,因为二氧化碳能够溶于水,并且能和水反应生成碳酸.
(3)请你另外设计一个方案,进一步探究变质情况
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量样品于试管中,加入足量水溶解,加入足量的氯化钙溶液,静置后滴加酚酞试液 | 产生白色沉淀,溶液变红色 | 猜想2成立 |
15.2017年4月15日是我国第二个“全民国家安全教育日”.下列说法正确的是( )
| A. | 煤矿的矿井不能通风,防止氧气进入 | |
| B. | 酒精能破坏蛋白质结构,可用于杀菌消毒 | |
| C. | 厨房天然气泄露,可用油烟机排气 | |
| D. | 久未开启的地窖,可直接进入 |
13.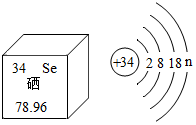 亚硒酸钠(Na2SeO3)可用于提升人体免疫力,硒元素由防癌、抗癌的作用,它在元素周期表的部分信息记原子结构示意图如图所示,下列说法不正确的是( )
亚硒酸钠(Na2SeO3)可用于提升人体免疫力,硒元素由防癌、抗癌的作用,它在元素周期表的部分信息记原子结构示意图如图所示,下列说法不正确的是( )
 亚硒酸钠(Na2SeO3)可用于提升人体免疫力,硒元素由防癌、抗癌的作用,它在元素周期表的部分信息记原子结构示意图如图所示,下列说法不正确的是( )
亚硒酸钠(Na2SeO3)可用于提升人体免疫力,硒元素由防癌、抗癌的作用,它在元素周期表的部分信息记原子结构示意图如图所示,下列说法不正确的是( )| A. | Na2SeO3中Se化合价为+4 | B. | n的值为6 | ||
| C. | Se是一种金属元素 | D. | Se的相对原子质量为78.96 |
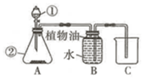 如图是小华同学设计的气体制取和收集装置,请你和他一起回答下列问题:
如图是小华同学设计的气体制取和收集装置,请你和他一起回答下列问题:



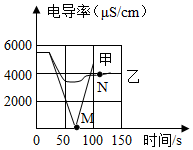 某化学兴趣小组通过探究活动学习和理解化学知识.请你一起研究学习,并回答有关问题.
某化学兴趣小组通过探究活动学习和理解化学知识.请你一起研究学习,并回答有关问题.