题目内容
8. 某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.
某化学兴趣小组的同学用如图所示装置进行实验(装置气密性良好),先关闭止水夹,将足量的氢氧化钠溶液滴入烧瓶中,充分吸收掉二氧化碳后,再打开止水夹.(1)烧瓶中观察到的现象是石灰水倒吸入烧瓶内,烧瓶内有白沉淀生成.澄清石灰水倒吸入烧瓶,烧瓶中溶液变浑浊
(2)根据上述现象能否得出“二氧化碳与氢氧化钠发生了反应”的结论?原因是不能,也可能是二氧化碳溶于水造成的.
(3)实验结束后,兴趣小组提出新问题:烧瓶内液体的溶质可能是什么?
[猜想]猜想①:溶质只有氢氧化钠;
猜想②:溶质是氢氧化钠和氢氧化钙;
你还需补充的猜想:溶质是氢氧化钠和氢氧化钙.氢氧化钠和碳酸钠.
[设计实验]请你为补充的猜想设计实验验证方案
| 实验操作 | 预期现象及结论 |
| 从烧瓶内取少量反应后的澄清溶液,向其中滴加碳酸钠溶液 | 白色沉淀生成,猜想②成立 |
分析 (1)根据二氧化碳和氢氧化钙的性质来判断反应现象;
(2)根据二氧化碳可以溶于水的性质进行分析;
(3)根据所加入的物质及它们的反应可以判断出可能存在的物质,但是碳酸钠和氢氧化钙不可能同时存在等知识进行分析.
解答 解:(1)二氧化碳可以和氢氧化钠反应,所以将氢氧化钠溶液滴入二氧化碳中,由于消耗了二氧化碳而使锥形瓶中气体压强变小,从而使试管中的石灰水进入锥形瓶,氢氧化钙溶液可以和二氧化碳或是碳酸钠反应生成碳酸钙沉淀,所以锥形瓶中的溶液要变浑浊;
(2)仅凭(1)中的现象不足以说明氢氧化钠溶液和二氧化碳发生了反应,因为氢氧化钠溶液中的溶剂为水,二氧化碳可以溶于水也会使锥形瓶中压强变小,且二氧化碳也能够使石灰水变浑浊,而产生(1)中现象;
(3)根据二氧化碳、氢氧化钠和氢氧化钙的化学性质,同时由于加入的氢氧化钠是足量的,所以可以判断在该溶液中溶质一定有氢氧化钠,可能存在的溶质为碳酸钠、氢氧化钙中的一种,注意碳酸钠和氢氧化钙不可能同时存在,因为碳酸钠可以和氢氧化钙发生反应生成碳酸钙和氢氧化钠,所以可以根据它们的性质来设计实验加以验证.
故答案为:(1)石灰水倒吸入烧瓶内,烧瓶内有白沉淀生成;
(2)二氧化碳溶于水也会产生相似的现象;
(3)Na2C03 和Na0H,
| 实验操作 | 实验现象 | 结论及反应的方程式 |
| 碳酸钠溶液 | 白色沉淀生成 | Na2CO3+Ca(0H)2═2Na0H+CaC03↓ |
点评 此题通过中和反应考查了化学方程式的书写,实验方案设计、实验操作以及实验方案的评价,解答时要全面审题,认真解答.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
16.下列物质中,属于纯净物的是( )
| A. | 食用醋 | B. | 干冰 | C. | 含碘盐 | D. | 可乐饮料 |
17.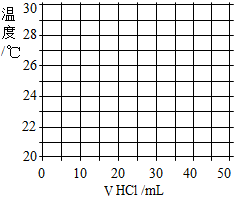
(1)据表可知V盐酸:VNaOH溶液=3:2时,两溶液恰好完全反应.由此可知NaOH溶液的浓度是0.6g/ml.
(2)当V盐酸:VNaOH溶液=1:4时溶液中含有的微粒有H2O、Na+、Cl-,、OH-(填符号).
(3)用铅笔在给定的坐标图上绘出溶液温度与盐酸体积的曲线图.并分析曲线变化的原因:开始时氢氧化钠和盐酸反应放热,溶液温度升高;当盐酸过量后,加入的过量的温度较低的盐酸使溶液温度降低.

| 盐酸的体积V(mL) | 5.0 | 10.0 | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 | 40.0 | 45.0 |
| NaOH的体积(mL) | 45.0 | 40.0 | 35.0 | 30.0 | 25.0 | 20.0 | 15.0 | 10.0 | 5.0 |
| 溶液温度t(℃) | 22.2 | 23.3 | 24.6 | 25.8 | 27.0 | 27.8 | 26.1 | 24.4 | 22.8 |
(2)当V盐酸:VNaOH溶液=1:4时溶液中含有的微粒有H2O、Na+、Cl-,、OH-(填符号).
(3)用铅笔在给定的坐标图上绘出溶液温度与盐酸体积的曲线图.并分析曲线变化的原因:开始时氢氧化钠和盐酸反应放热,溶液温度升高;当盐酸过量后,加入的过量的温度较低的盐酸使溶液温度降低.
3.下列实验方案的设计中,可行的是( )
| A. | 除去CO2中的CO气体可将其点燃 | |
| B. | 为检验CaO中是否含有Ca(OH)2,可将其加水后滴加酚酞溶液 | |
| C. | 用Ba(OH)2溶液可鉴别NH4Cl、H2SO4、(NH4)2SO4、HCl四种无色溶液 | |
| D. | 为除去炭粉中的CuO,可将其在空气中灼烧 |
18.下列生活中的各物质属于纯净物的是( )
| A. | 99.99%的黄金 | B. | 食醋 | C. | 可乐饮料 | D. | 加碘盐 |