题目内容
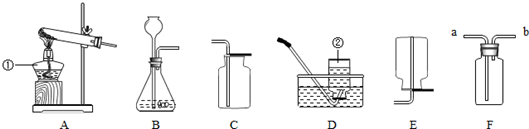
某校化学兴趣小组的同学根据实验室提供的仪器和药品,在老师的指导下从图中选择装置进行了氧气的制备实验.

(1)写出仪器a的名称: .
(2)甲同学从图中选择B、E装置的组合制取氧气,反应的表达式为: ,收集氧气还可选用的装置是 .若用图中A、E装置的组合制取氧气其表达式为 .
(3)乙同学称取一定质量的高锰酸钾固体放入大试管中,管口塞一团棉花,将温度控制在250℃加热制取氧气.实验结束时,乙同学发现用排水法收集到的O2大于理论产量.针对这一现象,同学们进行了如下探究:
【提出猜想】猜想I:反应生成的二氧化锰分解放出氧气;
猜想Ⅱ:反应生成的锰酸钾分解放出氧气;
猜想Ⅲ:反应生成的锰酸钾和二氧化锰分解都放出氧气.
【实验验证】同学们分成两组,分别进行下列实验:
第一组同学取一定质量的二氧化锰,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变,则猜想 错误;第二组同学取锰酸钾在250℃条件下加热,没有用测定质量的方法得出了猜想II正确的结论.该组同学选择的实验方法是 .
【拓展延伸】实验发现,氯酸钾固体加热制取氧气的反应速率很慢,但如果 将高锰酸钾固体与氯酸钾固体混合加热,则氯酸钾的分解速率大大加快.其原因是: ;高锰酸钾在该反应中 (填:“是”或“不是”)催化剂,理由是: .

(1)写出仪器a的名称:
(2)甲同学从图中选择B、E装置的组合制取氧气,反应的表达式为:
(3)乙同学称取一定质量的高锰酸钾固体放入大试管中,管口塞一团棉花,将温度控制在250℃加热制取氧气.实验结束时,乙同学发现用排水法收集到的O2大于理论产量.针对这一现象,同学们进行了如下探究:
【提出猜想】猜想I:反应生成的二氧化锰分解放出氧气;
猜想Ⅱ:反应生成的锰酸钾分解放出氧气;
猜想Ⅲ:反应生成的锰酸钾和二氧化锰分解都放出氧气.
【实验验证】同学们分成两组,分别进行下列实验:
第一组同学取一定质量的二氧化锰,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变,则猜想
【拓展延伸】实验发现,氯酸钾固体加热制取氧气的反应速率很慢,但如果 将高锰酸钾固体与氯酸钾固体混合加热,则氯酸钾的分解速率大大加快.其原因是:
考点:氧气的制取装置,氧气的收集方法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)从图中仪器a是锥形瓶去分析;
(2)从实验室制取氧气,B装置是固液不加热的发生装置,所以所用试剂应该是过氧化氢溶液和二氧化锰,因为氧气的密度比空气大,;A、E装置的组合装置的特点是加热固体制取气体,由于装置A中试管口没放棉花团,所以不能用加热高锰酸钾的方法制取氧气,只以用加热氯酸钾和二氧化锰的混合物的方法制取去分析;
(3)【实验验证】①从“第一组同学取一定质量的二氧化锰,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变”;我们还可以用验证氧气有无的方法去判断是否有氧气的生成去分析;
[拓展延伸]从加了高锰酸钾之后,产生氧气速度加快是因为高锰酸钾分解也会产生氧气,同时产生的二氧化锰对氯酸钾的分解起催化作用;但是由于在反应的过程中高锰酸钾的质量和化学性质都发生了改变去分析;
(2)从实验室制取氧气,B装置是固液不加热的发生装置,所以所用试剂应该是过氧化氢溶液和二氧化锰,因为氧气的密度比空气大,;A、E装置的组合装置的特点是加热固体制取气体,由于装置A中试管口没放棉花团,所以不能用加热高锰酸钾的方法制取氧气,只以用加热氯酸钾和二氧化锰的混合物的方法制取去分析;
(3)【实验验证】①从“第一组同学取一定质量的二氧化锰,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变”;我们还可以用验证氧气有无的方法去判断是否有氧气的生成去分析;
[拓展延伸]从加了高锰酸钾之后,产生氧气速度加快是因为高锰酸钾分解也会产生氧气,同时产生的二氧化锰对氯酸钾的分解起催化作用;但是由于在反应的过程中高锰酸钾的质量和化学性质都发生了改变去分析;
解答:解:(1)图中仪器a是锥形瓶.故答案为:锥形瓶;
(2)实验室制取氧气,B装置是固液不加热的发生装置,所以所用试剂应该是过氧化氢溶液和二氧化锰,反应的方程式为:2H2O
2H2O+O2↑;因为氧气的密度比空气大,因此还可以采用向上排空气法收集;A、E装置的组合装置的特点是加热固体制取气体,由于装置A中试管口没放棉花团,所以不能用加热高锰酸钾的方法制取氧气,只以用加热氯酸钾和二氧化锰的混合物的方法制取,加热氯酸钾和二氧化锰的混合物,生成氯化钾和氧气,其化学方程式为:2KClO3
2KCl+3O2↑;
故答案为:2H2O
2H2O+O2↑ C 2KClO3
2KCl+3O2↑;
(3)【实验验证】①根据“第一组同学取一定质量的二氧化锰,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变”说明二氧化锰没有发生反应,不是二氧化锰产生的氧气,所以猜想I和Ⅲ是错误的;我们还可以用验证氧气有无的方法去判断是否有氧气的生成,如用带火星的木条,伸入收集的气体中,如果木条复燃说明有氧气生成.
故答案为:I、Ⅲ检验是否有氧气生成;
[拓展延伸]加了高锰酸钾之后,产生氧气速度加快是因为高锰酸钾分解也会产生氧气,同时产生的二氧化锰对氯酸钾的分解起催化作用;但是由于在反应的过程中高锰酸钾的质量和化学性质都发生了改变,所以不是催化剂;故答案为:高锰酸钾受热分解生成氧气的同时,生成的二氧化锰是氯酸钾反应的催化剂 不是 高锰酸钾在反应前后质量和化学性质都发生了改变.
(2)实验室制取氧气,B装置是固液不加热的发生装置,所以所用试剂应该是过氧化氢溶液和二氧化锰,反应的方程式为:2H2O
| ||
| ||
| △ |
故答案为:2H2O
| ||
| ||
| △ |
(3)【实验验证】①根据“第一组同学取一定质量的二氧化锰,在250℃条件下加热一段时间,冷却后测得二氧化锰的质量不变”说明二氧化锰没有发生反应,不是二氧化锰产生的氧气,所以猜想I和Ⅲ是错误的;我们还可以用验证氧气有无的方法去判断是否有氧气的生成,如用带火星的木条,伸入收集的气体中,如果木条复燃说明有氧气生成.
故答案为:I、Ⅲ检验是否有氧气生成;
[拓展延伸]加了高锰酸钾之后,产生氧气速度加快是因为高锰酸钾分解也会产生氧气,同时产生的二氧化锰对氯酸钾的分解起催化作用;但是由于在反应的过程中高锰酸钾的质量和化学性质都发生了改变,所以不是催化剂;故答案为:高锰酸钾受热分解生成氧气的同时,生成的二氧化锰是氯酸钾反应的催化剂 不是 高锰酸钾在反应前后质量和化学性质都发生了改变.
点评:考点主要考查气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.

练习册系列答案
相关题目
吸烟有害健康.医学研究表明,肺癌、心脑血管病、冠心病等25种危及生命和健康的疾病,都与吸烟有关,全世界每年有400万人因吸烟而死亡.尼古丁是烟草产生的危害性最大的物质之一,当它的量达到40~60mg时,就能使一个成年人死亡.尼古丁的化学式可表示为:C10H14N2,下列关于尼古丁的说法中,不正确的是( )
| A、尼古丁中氢元素含量是氮元素含量的一半 |
| B、尼古丁中含26个原子 |
| C、尼古丁中碳、氢、氮元素的质量比为60:7:14 |
| D、尼古丁的相对分子质量为162 |
下列粒子中示意图中,表示-2价阴离子的是( )
A、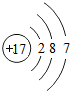 |
B、 |
C、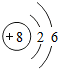 |
D、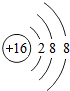 |
下列对金属和金属材料的认识中,错误的是( )
| A、回收废旧金属有利于节约金属资源 |
| B、铁粉作双吸剂和铁生锈的原理相同 |
| C、赤铁矿的主要成分是Fe2O3 |
| D、生铁和钢的性能完全相同 |
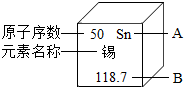 化学用语是最简明、信息丰富、国际通用的语言.
化学用语是最简明、信息丰富、国际通用的语言.